위산 분비에 있어서 히스타민의 역할
1920년에 폴란드의 생리학자인 Popielski가 히스타민이 위산의 분비를 자극한다고 보고하였다. 그 당시의 많은 연구자들은 가스트린이 실제적으로는 히스타민이라고 믿고 있었다. 1938년에 와서야 Komarov박사에 의하여 위 점막에서 분비를 촉진하는 두개의 서로 다른 물질이라는 것이 밝혀졌다. Komarov박사는 trichloroacetic acid를 이용하여 위점막 추출물에서 상청액(supernatant)에 있는 히스타민과 분리된 펩타이드인 가스트린을 분리해 내는데 성공했다. MacIntosh박사는 히스타민이 위산 분비의 최종적인 공통 매개체(final common mediator)라는 가설을 발표했다. 그는 가스트린과 아세틸콜린이 히스타민을 분비하고 그 결과 벽세포를 히스타민이 직접 자극하며, 히스타민만이 벽세포를 직접 자극하는 유일한 물질이라고 발표했다.
 이 시점에서 강화(potentiation)라는 개념이 정의되고 소개되었다. 강화는 두 개의 물질이 동시에 투여되면 각각의 역가의 합보다 더 강한 작용이 나오는 것을 말한다. 위장관에서 특정한 분비반응은 두 개 이상의 agonist에 의하여 강화작용을 나타낸다. 위장에서 히스타민은 벽세포에서 가스트린과 아세틸콜린의 효과를 강화시킨다. 그 결과 소량의 자극이 함께 작용하면 흔히 거의 최대의 분비반응을 나타낼 수 있다. 강화가 일어나기 위해서는 표적세포(target cell)에서 자극 받을 수 있는 분리된 별개의 수용체가 존재해야 한다. 그러나 위산이 분비되는 경우를 보면 강화현상은 최종적인 공통 매개체(final common mediator)가설은 모순된다.
이 시점에서 강화(potentiation)라는 개념이 정의되고 소개되었다. 강화는 두 개의 물질이 동시에 투여되면 각각의 역가의 합보다 더 강한 작용이 나오는 것을 말한다. 위장관에서 특정한 분비반응은 두 개 이상의 agonist에 의하여 강화작용을 나타낸다. 위장에서 히스타민은 벽세포에서 가스트린과 아세틸콜린의 효과를 강화시킨다. 그 결과 소량의 자극이 함께 작용하면 흔히 거의 최대의 분비반응을 나타낼 수 있다. 강화가 일어나기 위해서는 표적세포(target cell)에서 자극 받을 수 있는 분리된 별개의 수용체가 존재해야 한다. 그러나 위산이 분비되는 경우를 보면 강화현상은 최종적인 공통 매개체(final common mediator)가설은 모순된다.
처음 발견된 항히스타민은 기관지 수축과 혈관을 확장시키는 작용을 하는 히스타민 수용체 1(H1)을 차단하는 것이었다. 히스타민에 의하여 위산의 분비가 자극되는 것은 히스타민 수용체 2(H2)를 매개하여 작용하기 때문에 기존의 항히스타민제에 의해서는 차단되지 않는다. H2 수용체 길항제인 시메티딘(cimetidine)은 효과적으로 히스타민의 자극에 의한 산의 분비를 억제한다. 그러나 시메티딘은 가스트린, 아세틸콜린에 의한 것이나 음식물을 섭취했을 때 나오는 위산분비도 억제한다. 아트로핀(atropine)은 아세틸콜린의 muscarinic 수용체의 길항제인데 가스트린, 히스타민뿐만 아니라 아세틸콜린에 의한 위산의 분비도 감소시킨다. 실험적으로 다른 자극을 배제시키기 위하여 벽세포만 분리시켜서 실험한 결과, 가스트린 및 아세틸콜린 수용체를 자극해서 분비하는 것에 대한 시메티딘의 효과는 히스타민의 강화(potentiation) 작용에 의하여 분비 반응의 일부를 억제하기 때문이다. 비슷하게, 아트로핀에 의한 가스트린 및 히스타민의 분비 효과가 억제되는 것은 아세틸콜린의 강화작용이 제거되기 때문이다. 시메티딘은 아트로핀보다 부작용이 적으며 위산의 분비를 더 효율적으로 억제한다. 그래서 시메티딘은 십이지장의 소화성 궤양의 치료에 매우 효과적인 약으로 알려져 왔다.
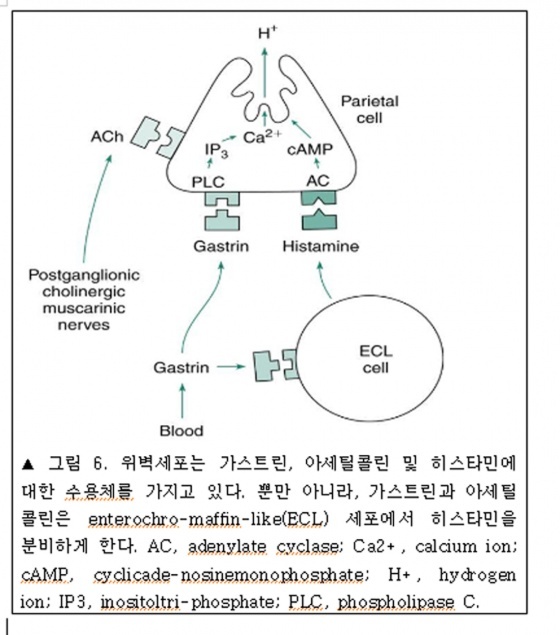
히스타민은 위벽 분비선의 lamina propria안의 entero-chromaffin-like(ECL)세포에서 발견된다. 가스트린, 히스타민 및 아세틸콜린의 상호 관계는 그림 6을 참고하면 도움이 된다. 벽세포 가까이 위치한 ECL세포는 히스타민을 분비하는데, 이것은 위산을 분비하는데 있어서 paracrine역할을 한다. ECL세포는 히스타민의 분비를 자극하고 ECL세포의 성장을 자극하는 가스트린에 대한 cholecystokinin-2(CCK-2)수용체를 가지고 있다. ECL세포는 아세틸콜린 수용체를 가지고 있지는 않다. 벽세포막은 히스타민, 아세틸콜린 및 가스트린의 3가지 모두에 대한 수용체를 가지고 있다. 벽세포는 히스타민의 H2 수용체, muscarinic수용체(M3) 및 가스트린/CCK-2 수용체를 가지고 있다. 비록 가스트린과 아세틸콜린이 위산분비에 있어서 중심적인 역할을 하지만 히스타민이 없으면 벽세포의 위산분비기능은 약화된다.
가스트린과 아세틸콜린은 phospholipase C(PLC)를 활성화 시키는데 이것은 inositol triphosphate(IP3)를 형성하는데 촉매역할을 한다. IP3는 세포내의 칼슘이온을 방출하고 calmodulin kinase를 활성화시킨다. 히스타민은 adenylate cyclase(AC)를 활성화 시켜서 cyclic adenosine monopho-sphate(cAMP)를 만들게 하는데, 이것이 protein kinase A를 활성화 시킨다. Protein kinase A 와 calmodulin kinase는 분비를 유도하는 다양한 단백질을 인산화시키고 각각의 다른 여러 가지 효과를 강화시킨다. 그러므로 시메티딘 같은 히스타민 H2 차단제에 의한 위산의 분비가 억제되는 것은 히스타민의 증폭된 상호작용을 제거하고 가스트린의 분비에 의한 히스타민의 자극을 억제하기 때문이다.
위산 분비의 자극
자극이 없는 상태의 사람의 위는 최대로 자극 받았을 때의 10`~15%정도의 위산을 분비한다. Basal acid secretion은 하루 동안에도 일주기의 변화가 있는데 저녁때 가장 많이 분비되고 아침에 깨기 직전이 가장 낮게 분비된다. 일주기의 변화가 있는 이유는 잘 모르나 혈중 가스트린 농도는 상대적으로 식간에 일정하게 분비된다. 위가 음식물을 소장으로 내려 보내고 나면 상대적으로 적은 위액만을 가지고 있고 위액의 산도(pH)는 보통 2이하이다. 그러므로 음식물이 없는 상태에서도 위점막은 산성상태를 유지한다.
위의 분비를 자극하는 것은 분비 반응을 시작하는 수용체의 위치에 근거하여 세단계로 편의상 나누고 있다. 이러한 분류는 인위적이기는 하나 음식을 먹고 조금만 시간이 경과하면 자극이 동시에 세 단계에서 시작되기 때문이다.
Cephalic Phase
혀와 입의 점막 및 비강 내에 있는 화학적 수용체와 기계적 수용체는 음식을 시음하거나 씹거나 삼킬 때 자극된다. 구심성 신경은 미주신경핵을 거쳐서 위에 원심성 신경을 내보낸다. 식욕을 증가시키는 음식을 생각하거나 보기만 해도 위산의 분비가 촉진된다. 뇌의 자극에 의한 분비반응은 음식의 종류에 따라 많이 달라진다. 본인이 선택한 입맛이 당기는 음식에서 가장 강력한 반응을 나타낸다. 특별히 맛이 당기지 않는 음식에서 가장 반응이 약하다. cephalic phase에서 원심성경로는 미주신경을 통해서 이루어진다. 이 반응은 미주신경 절제술을 하면 차단된다.
cephalic phase는 소위 가짜 먹이(sham feeding)를 이용한 방법으로 실험이 많이 이루어졌다. 실험용 개에서 위와 식도에 누공을 만들어 체외로 꺼내놓고 음식을 삼키게 하면서 음식이 식도에서 밖으로 빠져 나오게 하여 위에는 도달하지 못하게 하면서 위의 분비물을 누공을 통해서 모아서 그 분비물의 양과 위산의 정도를 측정한다. cephalic phase때의 자극은 음식물에 대한 전체 반응의 약 30%정도를 차지한다. 또한 cephalic phase에 대하여 여러 가지 다양한 약제를 이용한 연구도 이루어 졌다. tolbutamide나 인슐린을 투여하여 저혈당을 만들거나, 포도당과 유사한 3-methylglucose나 2-deoxyglucose를 투여하여 포도당의 대사를 방해하면 시상하부의 중심이 활성화되는데, 그 결과 미주신경을 자극하여 분비를 자극하게 된다.
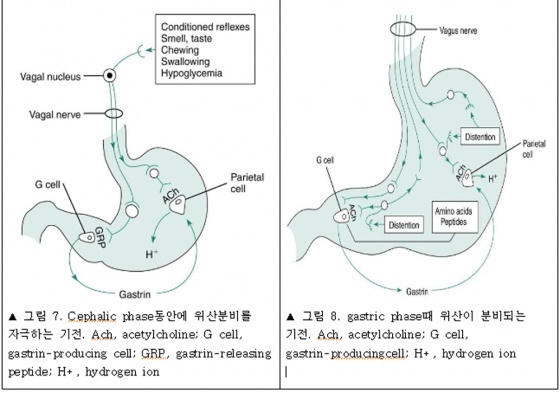
미주신경은 직접적으로 벽세포를 자극하여 위산의 분비를 촉진시킨다. 미주신경은 위 전정부(antrum)의 G세포(Gastrin cell)를 자극하여 가스트린은 분비한다. 벽세포를 자극하는 신경전달물질은 아세틸콜린이다. G세포의 매개체는 가스트린 분비 펩타이드(gastrin-releasing peptide, GRP)나 bombesin이다. 위 전정부에서 후신경절 미주신경은 자극 과 억제를 시키는 신경전달물질을 분비한다. 이러한 과정은 모두 밝혀져 있지는 않지만, 전체적인 반응은 복합적인 과정의 결과라고 할 수 있다. 벽세포에 대한 직접적인 효과는 인간에서 더 중요하다. 왜냐하면 위에서 벽세포가 있는 곳에 선택적인 미주신경절제술을 하면 가짜 먹이에 대한 반응이 나오지 않는다. 그러나 위의 전정부를 제거하면(antrectomy) 부분적으로만 위산의 분비가 감소된다. cephalic phase에 대한 기전은 그림 7을 참조하면 도움이 된다.
Gastric Phase
gastric phase때 위산의 분비는 약 50%에서 음식물의 영향을 받는다. 삼킨 음식물이 처음에 위에 들어가면 소량의 위액과 섞이게 되고 주로 음식물에 들어있는 단백질이 buffer역할을 해서 위산을 중화한다. 이때 위의 내용물의 pH는 6이상까지 올라간다. 위 전정부의 pH가 3이하로 떨어지면 가스트린의 분비가 억제되고 pH가 2이하로 떨어지면 음식물이 없는 위에서는 가스트린은 분비되지 않는다. pH가 올라가면 cephalic phase에 의하여 미주신경이 자극되고 gastric phase로 부터 자극되어 유지되면서 가스트린이 분비된다. 위의 pH가 증가되면 그 자체가 가스트린의 분비를 자극하는 것이 아니고 단지 다른 자극들이 효과적이 될 수 있게 해준다.
위가 팽창하고 위점막이 아미노산, 펩타이드나 아민같은 특정한 화학물질에 노출되면 gastric phase의 효과적인 자극이 된다. 위가 팽창하면 oxyntic 및 pyloric gland영역의 점막에서 미주신경을 통한 위벽 근육의 장단기 반사에 의하여 기계적 수용체가 활성화 된다. 이러한 팽창에 의한 반사는 아세틸콜린에 의하여 매개되고 아트로핀에 의하여 차단된다. 위점막의 팽창 수용체는 구심성 미주신경을 통해서 미주신경핵에 신호를 보낸다. 그 결과 원심성 미주신경은 G세포 및 벽세포에 신호를 보낸다. 국소반사는 위벽 내에 있는 신경에 의하여 이루어진다. 이러한 국소반사는 수용체(receptor)와 작용체(effector)가 위장의 동일부위에 위치한다는 뜻이다. 미주신경이 분포된 위의 전정부가 팽창하면 가스트린의 분비를 자극한다. 미주신경을 차단하면 이러한 반응은 감소하지만 없어지지는 않는다. 이러한 의미는 가스트린의 분비가 미주신경반사뿐만 아니라 국소반사에 의해서도 이루어지기 때문이다. 이러한 국소반사를 유문유문반사(pyloropyloric reflex)라고 한다.
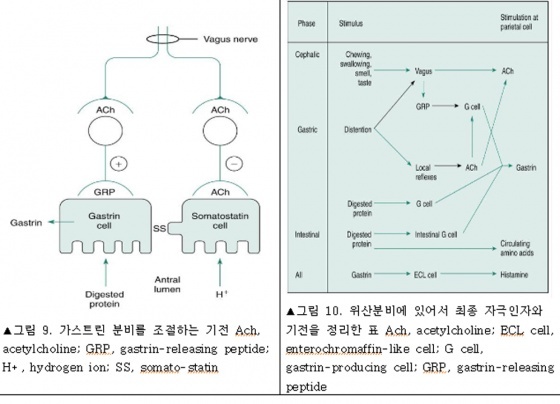
위의 pH가 1정도가 되면서 위의 전정부가 팽창하면 oxyntic gland area에 위산의 분비를 촉진한다. 원래 위의 pH가 2이하로 내려가면 가스트린은 분비되지 않기 때문에 이때의 위산분비는 신경반사에 의한 것이다. 이러한 미주신경반사를 pyloro-oxyntic reflex라고 부른다. 팽창에 의한 반사는 G세포보다는 벽세포에 더 효과적인 자극인데 그림 8에 잘 도식화 되어 있다.
펩타이드와 아미노산은 G세포에서 가스트린의 분비를 자극한다. 특히 가장 강력한 분비는 방향족 아미노산(aromatic amino acids)이다. 이것은 미주신경절제술에 의하여 차단되지 않는다. 이것은 부분적으로 아트로핀에 의하여 차단되는데 이러한 결과는 단백질의 소화 결과물은 직접적으로 가스트린의 분비를 자극하는 물질을 포함하고 있다는 뜻이다. 위 전정부의 점막이 pH가 3이하로 산성화되면 소화된 단백질의 자극에 의한 가스트린의 분비도 억제된다. 카페인 유무에 상관없이 섭취한 커피나, 위속에 있거나 증가된 혈중 칼슘이온은 위산의 분비를 촉진한다. 알코올이 위산의 분비에 미치는 영향은 많은 논란이 있다. 다른 동물에서는 알코올이 가스트린과 위산의 분비를 촉진하지만 인간에서는 그렇지 않았다.
가스트린의 분비
많은 연구를 통해서 밝혀진 가스트린의 분비를 조절하는 기전은 그림 9에 잘 도식화 되어있다. GRP(gastrin-releasing peptide)은 G세포에 작용하여 가스트린의 분비를 자극하고 somatostatin은 G세포에 작용하여 가스트린의 분비를 억제한다. GRP는 미주신경 자극에 의하여 분비되는 neurocrine이다. 이러한 현상은 아트로핀이 미주신경을 매개해서 분비하는 가스트린을 차단하지 못하는 이유가 된다. somatostatin은 paracrine처럼 작용하는데 이것의 분비는 미주신경의 자극에 의하여 억제된다. 종합하여보면 미주신경이 활성화 되면 GRP를 분비하고 somatostatin의 분비를 억제하여 가스트린의 분비를 촉진한다. 그리고 가스트린 자체가 음성 되먹임으로 somatostatin의 분비를 증가시킨다.
위산이 직접적으로 somatostatin 세포를 자극하여 soma-tostatin의 분비를 촉진하여 가스트린의 분비를 억제하게 된다. 단백질의 소화 산물인 펩타이드, 아미노산 및 아민들은 G세포에 직접적으로 작용하거나 G세포에 의하여 흡수되어 가스트린의 분비를 촉진한다.
Intestinal Phase
위점막의 신경을 차단한 경우에도 단백질이 소화되어 십이지장에 도달하면 위산이 분비되는데 이것은 호르몬도 위산분비에 관여한다는 뜻이 된다. 십이지장 근위부에는 가스트린을 분비하는 세포가 풍부한데 그 결과 음식을 먹으면 혈중 가스트린에 영향을 준다.
또한 정맥으로 아미노산은 주입하면 위산의 분비가 촉진된다. 그러므로 intestinal phase에서 상당한 양의 위산의 분비는 아미노산의 흡수에 의하여 일어날 수 있다. 그러나 음식을 먹어서 소장을 자극하여 분비되는 위산은 약 5%정도이다. 즉 gastric phase가 대부분의 위산 분비에 영향을 준다는 뜻이다.
<다음 호에 계속>

