
[엠디저널]알츠하이머는 정확히 말하면 질병이 아니며, 기억에 필요한 에너지를 사용하지 않으려는 뇌에 꼭 필요한 과정이다. 뇌의 방대하고 심오한 시냅스 네트워크가 뇌 보호 프로그램에 따라 진행된 뇌의 축소 작업의 결과이다. 다시 말하면, 안 좋아진 뇌 환경에서 생존을 위해 에너지를 많이 써야 하는 인지기능을 축소시켰을 뿐인데 뇌는 알츠하이머라는 질병을 얻는 것이다. “알츠하이머의 종말”의 저자 데일 브레드슨 박사는 알츠하이머 환자는 기억하고, 생각하고, 이해하고 상상하는 능력, 즉 인간답게 만드는 능력을 생명을 유지하기 위해 포기한다고 저술하고 있다.
우리가 원하거나 반기는 일은 아니지만 뇌는 생명을 연장하기 위해 우리의 의지와는 무관하게 뇌가 판단하기에 더 중요한 일에 우선순위를 두는 기억을 남기는 병증을 보이며 진행된다. APP가 수용체로부터 호르몬, 비타민, 영양소, 그 외에 시냅스를 유지하고 만드는데 필요한 분자가 부족하다고 신호를 받고 시냅스를 축소하라는 명령을 받으면 가장 최근의 기억부터 지운다. 이와 같은 내용은 핸드폰의 용량이 가득 찼을 때 더 중요한 사진을 저장하기 위해 아깝지만 지우기 싫은 이전의 저장된 사진을 지울 수밖에 없는 상황과도 같다.
알츠하이머 환자는 일상생활 활동에서 도움을 받기 위해 가족이나 전문 간병인에게 의존하는 정도가 점점 높아지게 되어 결국 요양원이나 다른 장기 간호시설에 들어갈 수밖에 없다. 질병의 진행기간으로 10년 이상 걸리는 경우가 많기 때문에, 막대한 사회적 및 재정적 부담을 안겨주며 가족 구성원에게 심각한 정서적 고통을 주고 있다.
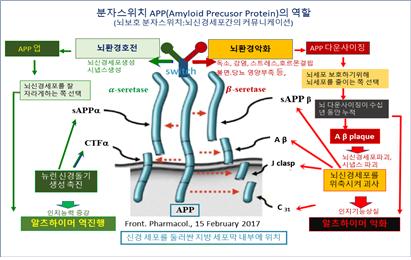
아밀로이드 전구체단백질(Amyloid Precusor Protein, APP)
아밀로이드 전구체단백질(Amyloid Precusor Protein, APP)은 알츠하이머의 원인으로 작용하는 Aβ를 생성하는 전 단계 물질로써 우리 뇌에서는 뇌를 보호하기 위한 분자 스위치 역할을 한다. 건강한 뇌에서 APP 분자스위치는 뇌 환경이 좋을 때 α-세크레타제가 작동하는 비아밀로이드 생성경로(Nonamyloidogenic Pathway)에서 새로운 뉴런을 생성하는 등의 생산적인 일을 하도록 작동한다. 반대로 균에 감염되었든지 중금속 등에 의한 독소에 노출되거나 영양결핍으로 뇌의 환경이 악화되었다고 판단될 때 뇌는 스스로를 최대한 보호하기 위해 뇌의 일을 줄이라는 신호를 보낸다. 이 신호를 받아 APP의 다운스위치에 불이 켜지면서 APP가 β-세크레타제와 γ-세크레타제 분해를 통해 Aβ를 생산하는 아밀로이드 생성경로(Amyloidogenic Pathway)를 시작한다(그림 1, 2).
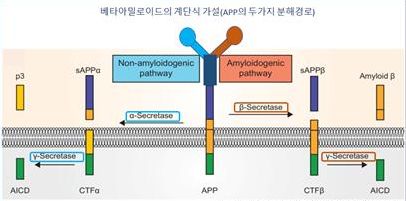
APP는 21번 염색체에서 확인된다. APP 유전자의 돌연변이는 α-세크레타제에 의한 정상적인 절단 대신 β- 및 γ-세크레타제에 의한 과도한 절단을 일으키며, EOAD(Early Onset Alzheimer’s Disease)에서 중요한 유전적 구성 요소로서 관여한다. 일반적으로 65세 이전에 발생하는 EOAD는 모든 알츠하이머 사례 중 6%~7%에 불과하다. 또한 알츠하이머 환자 전체의 13%만이 형제, 부모 및 조부모도 같은 질환을 앓고 있는 FAD(Familial Alzheimer’s Disease)에 해당된다.
알츠하이머의 증상 어떻게 진행되나?
(1) 기억력 감퇴
해마와 피질의 콜린성 신경이 퇴행화되어 인지기능을 감소시키며 기억력 감퇴는 알츠하이머의 초기부터 가장 흔하게 나타난다. 알츠하이머의 원인은 아직까지 정확히 알려지지 않았지만, 질병 발병은 대개 최근의 사건에 대한 기억 상실로 특징지어지며, 반복적인 질문과 새로운 개념을 익히는 능력의 상실로 이어지게 된다.
(2) 언어능력 저하
초기에는 말을 하려 할 때 적절한 단어가 떠오르지 않고 점차 언어를 구사하는데 적당한 단어를 찾기 힘들어지고 말문이 막히는 상황이 되면 입을 다물어버리는 경우가 종종 발생한다. 또한 언어장애가 생기기 시작하면 말 수도 줄게 되고 상대방의 말을 잘 이해하지 못하고 본인의 말만 주장하는 일이 자주 생기게 된다.
(3) 시공간파악 능력(지남력)의 저하
알츠하이머 초기에는 시간, 날짜나 요일을 잊는 일이 자주 반복되고 점차 중요한 약속이나 집안 중대사를 챙기지 못하게 된다. 더 심해지게 되면 낮과 밤을 혼동하거나 계절을 파악하지 못하고 계절에 맞지 않는 옷을 꺼내 입어 주위를 당혹스럽게 하기도 한다. 처음에는 익숙하지 않은 장소에서 혼동을 보이다가 증세가 심해지면 지나간 길을 다시 되돌아오지 못하고, 늘 다니던 익숙한 곳에서 길을 잃어버리는 일도 잦게 된다. 그러다가 결국에는 자신이 있는 곳이 어디인지 전혀 알지 못하게 되고, 함께 지내는 배우자나 가족을 알아보지 못하고 과거의 기억 속의 인물을 찾아 헤맨다.
(4) 판단력 및 일상생활 수행능력의 저하
숨 쉬고 체온을 조절하는 방법을 기억하기 위해 어제 친구와 있었던 사소한 다툼의 기억을 포기하거나 새로운 기억은 포기하고, 나에게 가장 소중한 기억을 살린다. 생활에 필요한 중요한 업무나 취미에 관련된 기술 즉, 반복되는 작업을 선택한다. 그렇지만 이 작업이 우리에게는 좋지 않을 수도 있다. 결국에는 양치질하기, 식사하기, 옷 갈아입기, 대소변 가리기 등 가장 기본적인 일상 활동들도 스스로 하지 못하게 된다. 호흡과 같은 기능마저 잃어버리면 환자는 사망에 이르게 된다.
(5) 정신행동증상
알츠하이머 환자는 인지기능장애뿐만 아니라 성격변화, 공격성 증가, 기분저하, 조울증, 공상, 환각, 불면 등 ‘정신행동증상’이 나타난다. 원래의 성격과 다르게 친구들과 잘 어울리지 않고 집에만 있거나, 의욕도 없고 질문에 대답도 하지 않고 멍하니 한 곳을 바라보며 깊이 사색을 한다거나 의기소침한 부분을 보이기도 하고 반면에 아주 사소한 일에도 짜증이나 화를 벌컥 내거나, 공격적인 거친 말과 행동을 거침없이 하게 된다.
또한 과거의 어떤 행복한 순간을 떠올리며 들떠서 한없이 기뻐하다 가도 주변사람에게 훔쳐간 물건을 내놓으라고 생 때를 쓰는 등 난처하게 만들기도 하고, 물건을 꽁꽁 싸매어 숨겨놓는다거나 자신을 해치는 사람들이 숨어 있다고 한 쪽 구석에 숨어 나오지 않는 등 망상에 사로잡히기도 하고 종잡을 수 없는 행동과 사고들이 가족과 돌보는 사람을 힘들게 한다. 그 밖에도 불면으로 고생하는가 싶다가도 밤이 되면 더 정신이 또렷해져서 일하러 밖으로 나가려고 하는 증상을 보이기도 한다.
(6) 신체 증상
알츠하이머가 더 심각하게 진행되면 대소변을 가리지 못하고, 몸이 경직되고 보행 장애가 나타나 걷기 힘들어진다. 거동 장애와 더불어 낙상으로 크게 다치기도 하고 오랜 침대생활로 인한 순환장애로 인해 욕창이 생겨 고생하기도 하고 방광염이나 요도 감염 등 감염에 노출되기 쉬우며 면역 약화 등의 신체적 문제가 합병증으로 나타나 사망에 이른다.
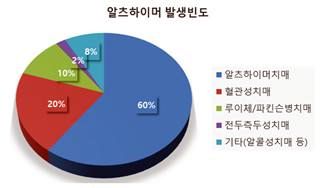
알츠하이머의 발생 빈도
현재까지 알려진 알츠하이머의 대표적인 병인은 노인 치매는 인지능력 저하를 수반하는 노인성 질환으로 최근 수십 년간 연구가 지속되어 오고 있지만 정확한 병리 기전은 확정된 것이 없다. 전 세계적으로 약 5천만 명 이상의 치매 환자가 존재하는 것으로 알려져 있으며 유병률은 증가하고 있다. 이 중에서 알츠하이머가 전체 치매환자의 약 60%의 비율을 차지하고, 혈관성치매 약 20%, 루이소체치매 약 10%, 전두측두엽치매가 약 2% 비율을 차지하고 있으며 이들이 치매의 일반적인 형태로 알려져 있다(그림 3).
알츠하이머의 경과 및 진단은?
초기에는 기억력 저하가 정신행동 증상(무관심, 우울, 불안 등)과 동반되어 나타날 수 있다. 이후 심각한 기억력 저하를 포함한 인지 기능의 현저한 저하가 나타나며, 일반적으로 정신행동 증상이 심해지는 경향을 보이며, 수면장애와 저녁이 되면서 혼돈이 심해지는 일몰증후군(Sundowning)이 나타나기도 한다.
주관적 인지 저하(Subjective Cognitive Decline, SCD)는 AD가 진행되는 중간 단계로써 정상(Cognition Normal, CN)과 경도인지장애(Mild Cognitive Impairment, MCI)의 중간 단계에 해당하며, 대부분의 경우 전임상 알츠하이머(preclinical AD, Pre-AD)도 SCD에 포함한다. AD 병리학, 특히 뇌 아밀로이드(brain amyloid)의 증거인 아밀로이드 양전자방출 단층촬영(Amyloid Positron Emission Tomography, PET) 또는 뇌척수액(CerebroSpinal Fluid, CSF)의 아밀로이드 검사로 경도인지장애(MCI) 환자를 Pro-AD로 진행할 가능성이 있는 환자로 규정짓는다.
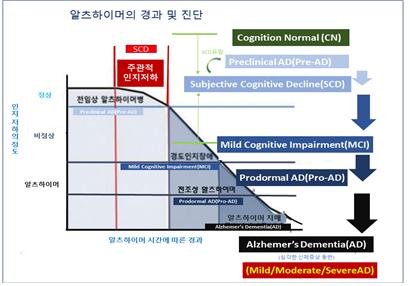
이러한 바이오마커(brain amyloid) 이상이 동반 된 MCI는 현재 Pro-AD로 진단된다. 연구에 의하면 상승된 아밀로이드가 인지 기능 악화의 위험과 관련되어 있어 5 ~ 6년 사이의 MCI 진행 위험도는 11%에서 56% 사이이며, 해마상 위축이나 CSF tau와 같은 신경 퇴행성 징후와 관련된 위험률이 높다고 알려져 있다. Pre-AD(SCD포함)의 개념은 노화와 알츠하이머의 이해와 약물 개발에 중요한 영향을 미친다. 흔히 중증 알츠하이머(Severe AD) 환자라고 하면 혼자 걸어 다닐 수는 있지만 스스로 옷을 입거나 목욕을 하고 대소변을 보는 일 등 반복적인 단순한 일상생활을 할 수 없는 경우를 말하며, 기억 및 인식 기능도 없다(그림 4).
알츠하이머의 진찰
알츠하이머 진단에 있어서는 환자에 대해 가장 잘 알고 있는 보호자의 보고를 통한 정확한 병력 청취가 매우 중요하다. 의사는 이전에 비해 기억력을 포함한 인지기능저하(cognition, C), 일상생활(직업, 사회생활)의 수행의 어려움(activities of daily living, ADL)들을 살피고, 이상 행동, 문제 행동(behavior, B), 원인 질환이 다양한 증상군(differential diagnosis, D)등의 특징이 있는지를 파악하며, 간이 정신 상태 검사(Korea Mini Mental State Examination, K-MMSE)와 알츠하이머병 인지 평가척도(Alzheimer’s Disease Assessment Scale-Cognitive Subscale, ADAS), 신경 심리 검사(Seoul Neuropsychological Screening Battery, SNSB), 일상 생활능력 평가(Activities of Daily Living, ADL), 신경 정신 행동 검사(NeuroPsychiatric Inventory, NPI)등으로 평가한 전반적 인지기능으로 환자를 진찰하고 진단한다.
CDR (Clinical Dementia Rating)은 치매의 중증도 평가의 기준이 되며 K-MMSE점수만으로는 치매의 중증도 판단의 어려움을 보완해주고, 치료과정에서 환자의 변화를 추적하는 기준설정, 적절한 약물의 선택 및 치료 계획 수립, 환자의 상태 및 경과, 치매 치료제의 국민건강보험 급여기준 확보, 간병 지침 그리고 치매 보험들의 보상기준 제공 등의 중요한 의의를 갖는다.
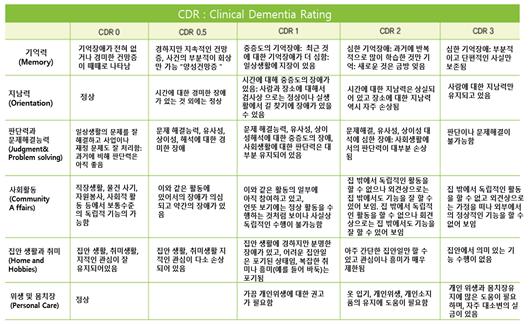
위의 표의 6가지 세부항목 1) 기억력 2) 지남력 3) 판단력과 문제해결능력 4) 사회활동 5) 집안 생활과 취미 6) 위생 및 몸치장 등에 대한 등급의 6가지 점수의 총 합을 1-30점으로 나누고 이를 Sum of Boxes(CDR-SB)라 한다(표 1).
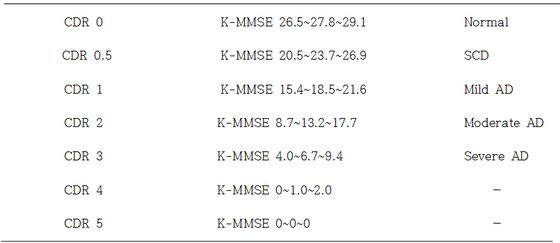
환자 및 보호자와 자세한 면담 후 평가 인지 장애로 인한 기능의 저하만을 평가하며 CDR 0: 정상(Normal), CDR 0.5: 경도인지장애(SCD), CDR 1: 경함(Mild), CDR 2: 중증도(Moderate), CDR 3: 심함(Severe)으로 나누고, CDR 0은 K-MMSE: 26.5~27.8~29.1 (정상), CDR 0.5는 K-MMSE: 20.5~23.7~26.9 (경도인지장애), CDR 1은 K-MMSE: 15.4~18.5~21.6 (경도치매), CDR 2는 K-MMSE: 8.7~13.2~17.7 (중증치매), CDR 3은 K-MMSE: 4.0~6.7~9.4 (심한치매), CDR 4는 K-MMSE: 0~1.0~2.0, CDR 5는 K-MMSE: 0~0~0으로 계산한다(표 2).
이와 같이 신체검사와 신경학적 검사, 정신상태 검사, 일상생활 기능수준 검사, 혈액 검사 등의 실험실 검사, 자기 공명 영상(MRI), 컴퓨터 단층 촬영(CT) 등 구조적 뇌 영상 검사와 양자 방출 단층 촬영(PET), 단일 광자 방출 촬영(SPECT) 등의 뇌 영상학 검사, 신경 심리 검사(SNSB) 등 모든 검사를 통해 진단을 내린다.
대부분의 경우 Pre-AD도 SCD에 포함하며 SCD는 정상과 MCI의 중간 단계에 해당한다. MCI는 기억 손상이 있지만 일상 활동이 극히 정상이고, 한 번씩 대화 장애가 있지만 치매 환자처럼 행동하지 않으며, 흔히 치매의 발병위험 단계로 이해하지만 모든 MCI 환자가 전부 AD로 진행되는 것은 아니다.
알츠하이머의 다양한 발병 원인
아래 그림은 알츠하이머의 병리 현상을 도식적으로 표현한 것으로 알츠하이머의 다원적인 난관을 묘사한다. 아래의 그림 5는 세포 외 아밀로이드 응집체의 형성에서 차례로 타우 응집체(tau aggregates) 및 신경섬유다발(NeuroFibrillary Tangles, NFT)을 형성하여 신경 세포 손실, 시냅스 기능 장애 및 알츠하이머의 특징인 뉴런의 손실에 기여하는 Aβ의 역할을 보여준다. 또한, 성상아교세포(astrocyte)의 periplaque 활성화는 다양한 사이토카인(CytoKine, CK)의 방출을 초래하고 미세아교세포(microglia)의 활성산소(superoxide, O2-)의 분비로 이어진다. 노화로 인해 손상된 미토콘드리아는 세포내 유리기(free radicles)를 제거하지 못하고 축적하여 신경 세포의 에너지 효율을 변경시킨다. 세포외독성 활성화(excitotoxic activity)에 의해 표현되는 Ca2+항상성(Ca2+ homeostasis)의 손실은 알츠하이머 병리에 핵심 역할을 할 수 있다. 또한 장내 미생물군총(microbiome) 구성의 변화도 알츠하이머 병인으로 작용할 수 있다.
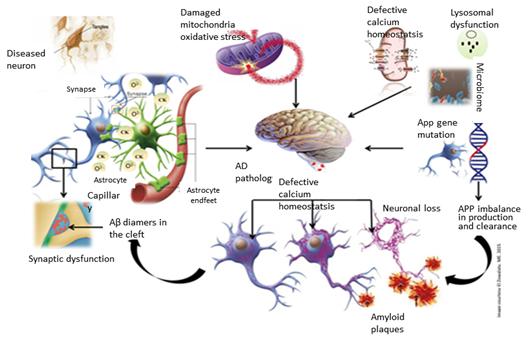
알츠하이머의 원인은 유전적 소인, 정신적 스트레스, CNS 감염, 장관 내 미생물군총(microbiome)의 이상 등 여러 가지 가설이 있으나 이 중 어떤 원인도 알츠하이머 발병 원인의 30% 이상을 설명할 수 없다. 결국, 다양한 원인에 의해 Aβ 생성이 증가하거나 oligomerization tendency가 증가하거나 Aβ의 제거가 저하되어 Aβ oligomer(OAβ)가 증가함으로써 알츠하이머가 발병한다고 보는 것이 알츠하이머 치료제를 개발하는 관점에서 가장 올바른 이해라고 볼 수 있다.
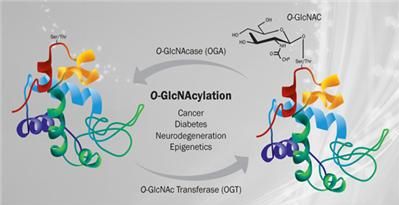
또한 국소적 포도당 대사 저하는 알츠하이머의 특징으로 포도당 대사 저하와 AD의 진행 사이에 하나의 새로운 연결 고리로 영양(nutrient) 즉, 반응하는 nucleocytoplasmic protein의 post-translational O-GlcNAcylation이 있다. O-GlcNAc(O-N-acetyl-glucosamine)는 뉴런에 풍부하고 타우 및 APP(아밀로이드 전구체 단백질) 모두 존재하며, 뇌는 GlcNAcylation이 증가될수록 타우 및 β-아밀로이드 펩타이드 독성으로부터 보호받는다. 알츠하이머에서는 O-GlcNAcylation이 감소되는 것을 발견할 수 있으며, 포도당 대사 저하가 뉴런 내에서 O-GlcNAc의 보호 역할을 손상시키고 신경 퇴행을 가능하게 할 수 있다(그림 6).
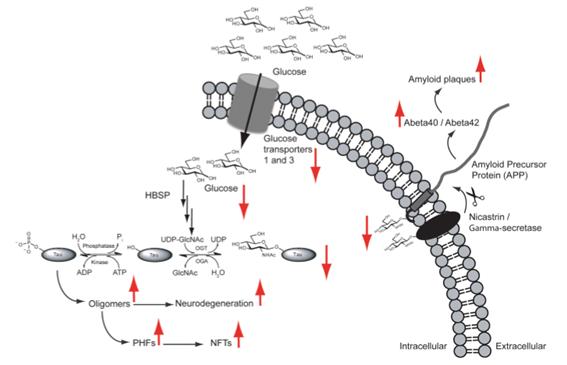
포도당 이용 장애(Impairments in glucose utilization) 다시 말하면, 세포 표면 글루코스 전달 인자modification(cell-surface glucose transporters) 감소는 헥소사민 생합성 경로(hexosamine biosynthetic pathway, HBSP)의 감소로 이어져 결국 tau, APP 및 nicastrin(γ-secretase 복합체의 구성 요소)에 대한 O-GlcNAc의 감소로 이어지며 이러한 상황은 알츠하이머 뇌의 특징인 NFT와 아밀로이드 플라크의 생성을 증가시킬 수 있다(그림 7).
따라서 식물유래 필수 탄수화물인 글리코 영양소의 풍부한 섭취에 의한 뇌의 Glycosylation은 알츠하이머의 고단한 일상으로부터 나를 구해줄 수 있는 멋진 대안이 될 수 있다.

