
[엠디저널]하룻밤 수면 부족이 뇌 ABB(Aβ burden)에 악영향을 미치고 만성적인 수면결핍(chronic less sleep)은 이전에 생성된 Aβ 축적을 가속화시킨다. 질병통제 예방센터는 뇌에서 Aβ 축적을 예방하는 전략으로 성인 1인당 최소 7시간의 수면을 권장하며, 안락한 환경에서 숙면을 취하는 건강한 수면의 질(deep non-REM sleep)을 확보하는 생활습관이 건강한 뇌를 간직하는 길이다.
만성적인 수면부족이 알츠하이머를 유발한다.
알츠하이머(AD)의 위험 인자로 수면과 β-아밀로이드(Aβ)와의 연관성에 대한 관심이 증가하고 있다. Aβ는 뇌의 간질액(Interstitial fluid, ISF)에 존재하고 대사성 폐기물로 인식되어 제거된다. 뇌에서 Aβ가 제거되는 메카니즘은 완벽하게 규명되지는 않았지만 수면이 Aβ의 제거에 중요한 역할을 한다. 설치류에서 만성 수면 제한은 ISF-Aβ 수치의 증가를 가져왔고, AD의 초파리 모델에서 만성 수면박탈(chronic sleep deprivation, CSD)은 더 높은 Aβ의 축적을 초래했으며, 건강한 사람의 경우 수면 지속시간이 짧거나 수면의 질이 좋지 않은(개인적인 느낌) 경우 AD의 위험요소인 뇌의 ABB(Aβ burden)가 더 높은 것으로 밝혀졌다(그림 1). 또한 수면 장애는 뇌에서 Aβ의 축적을 촉진하여 AD에 기여할 수 있다. 하룻밤 수면 부족이 뇌 ABB(Aβ burden)에 악영향을 미치고 만성적인 수면결핍(chronic less sleep)은 이전에 생성된 Aβ 축적을 가속화시킨다는 연구 결과가 있다.
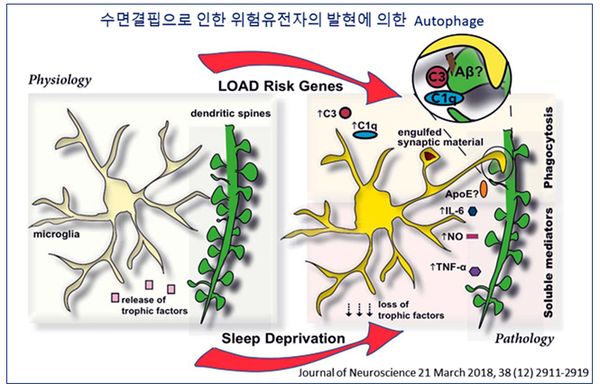
이 연구는 뇌의 수면 부족으로 인한 잠재적인 해로운 영향에 대한 새로운 통찰력을 제공하며 AD의 병리학을 보다 잘 특성화 할 수 있는 의의를 가지고 있다. 또한 Aβ 수치가 높아지면 수면 장애를 일으킬 수 있기 때문에 수면 장애와 AD 위험 사이의 연관성에 대해 양방향으로 고려되어야 한다. AD 환자의 불면에 수면제 처방은 큰 효과는 없으며, 밤에 충분히 잘 수 있게 낮에 다양한 활동을 할 수 있도록 배려하는 일이 중요하다. 불면은 또한 환각 등의 증세를 불러오기도 하므로 밤에는 숙면을 취할 수 있는 분위기를 만들어 주는 것이 제일 좋다. 따라서 뇌에서 Aβ 축적을 예방하는 전략으로 질병통제 예방센터는 충분한 수면시간으로 성인 1인당 최소 7시간의 수면을 권장하며, 안락한 환경에서 숙면을 취하는 건강한 수면의 질(deep non-REM sleep)을 확보하는 생활습관이 건강한 뇌를 간직하는 길이며 알츠하이머 예방에 중요할 수 있다는 점을 강조하고 있다(그림 2).
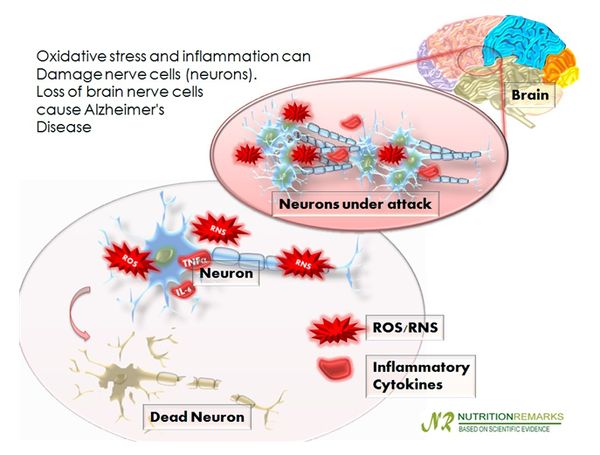
지속적인 스트레스가 알츠하이머를 유발한다.
모든 스트레스는 지울 수 없는 흉터를 남기며, 스트레스가 많은 상황에서 조금 더 오래 지내면 유기체는 생존을 위해 돈을 지불한다.
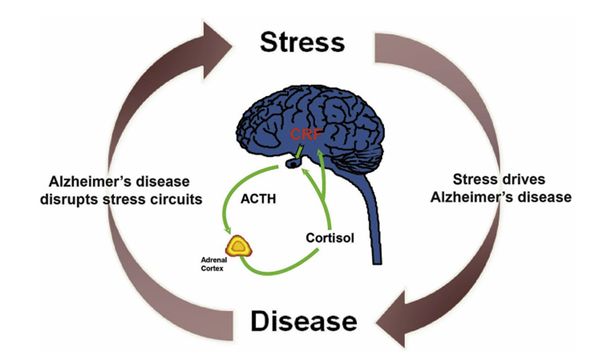
스트레스는 모든 질병의 발달과 진행에 밀접하게 관련되어 있다. 특히 인지기능과 운동기능의 상실감을 수반하는 신경 퇴행성 질환인 AD는 스트레스 반응을 중재하는 신경 회로를 파괴할 수 있다. 거기에 새로운 스트레스가 가해지면 스트레스 조절과정을 방해하여 AD의 진행을 촉진시키고 증상을 악화시킬 수 있다. 만성 스트레스가 AD의 진행을 가속화할 수 있으며, 또한 AD의 위험 인자로서 만성 스트레스를 손꼽는다. 만성적인 스트레스는 Aβ 축적, Tau의 과인산화, 산화 스트레스 및 미토콘드리아 기능부전과 같은 노화와 AD에 관여하는 것으로 알려진 과정의 일부를 돕는 방아쇠 역할로서 cortisol을 분비하여 AD의 증세악화 또는 발병을 증가시킬 수 있다. 또한 스트레스와 AD와의 feed-forward 관계를 "스트레스의 악순환”(“vicious cycle of stress”)이라고 한다(그림 3).
‘Vicious cycle of stress’는 스트레스가 질병을 유발하고 질병이 스트레스를 유발하여 질병 진행을 촉진하고 신경 정신계 합병증을 유발할 수 있다고 가정하여 스트레스와 AD와의 관계를 도식화하여 나타내고 스트레스가 어떻게 AD의 진행을 유도하는지 알기 쉽게 설명해준다. 과도한 스트레스가 AD의 진행을 촉진하며, 스트레스 패러다임에 의해 HPA축 활성도와 그에 상응하는 순환 cortisol 농도의 증가에 따라 AD의 발병이 좌우된다. 또한 높은 cortisol 농도는 뉴런 기능을 손상시키고 뉴런의 세포 사멸을 유도한다. 스트레스 또는 외인성으로 인한 cortisol의 상승은 Aβ, Aβ plaque, 유독한 용해성 OAβ 및 타우 단백질의 생산을 증가시켜 이러한 유해한 순환을 더욱 악화시킨다. 그러나 ‘Vicious cycle of stress’의 사이클이 스트레스가 AD에 영향을 줄 수 있는 모든 상황을 설명하지는 못한다. 스트레스를 받으면 우리 몸은 뇌를 보호하기 위해 APP(Amyloid Precursor Protein) 스위치를 다운사이징으로 끄고 스트레스를 해독하기 위해 Aβ를 만들고 생산적인 일을 줄이도록 명령한다. 또한 유독한 용해성 OAβ는 CRF 뉴런을 직접 흥분시켜 스트레스 반응을 일으킬 수 있으며, 또한 CRF 뉴런은 비정상적인 단백질인 Aβ의 존재를 감지하고 HPA축을 활성화시킴으로써 뇌에 무언가 부적합하다는 것을 우리 몸에 경고한다. 이어서 HPA축이 활성화되고 cortisol 분비라는 뇌의 단백항상성(proteostasis) 장애를 해결하기 위한 시도일 수 있는 일반화된 스트레스 반응을 구현한다(그림 4).
Cortisol 분비의 항상성 조절이 질병을 피해 가는데 중요한 역할을 하기 때문에 실제로 cortisol 농도 상승은 근본적인 AD 병리를 악화시킬 것으로 예측된다. 스트레스와 cortisol의 상관관계는 너무 적은 양의 스트레스나 너무 많은 양의 스트레스 둘 다 모두가 cortisol 분비에 해로운 영향을 줄 수 있는 “U 자형” 곡선을 종종 나타내는데, 이것은 cortisol이 높거나 낮은 경우 모두 높은 Aβ를 생성할 수 있다는 잠재적인 설명이 될 수 있다. 하지만 외상에 의한 HPA축의 변화와 알츠하이머 위험의 증가를 연결하는 메카니즘을 규명하기 위해서는 더 많은 연구가 필요하다.
콜레스테롤(Cholesterol) 저하 및 과잉이 알츠하이머를 유발한다.
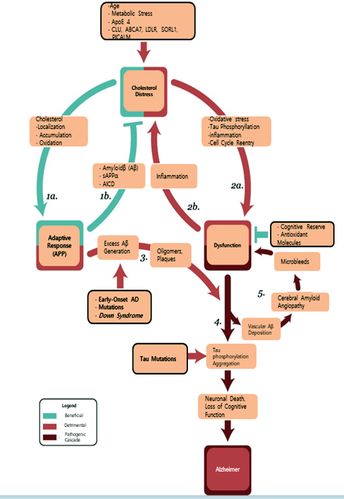
콜레스테롤 저하가 후기 발병 알츠하이머의 경우 Aβ 축적보다 오히려 병원성 유발인자(pathogenic trigger)일 가능성이 더 높다. 콜레스테롤 부조화(Cholesterol distress)는 콜레스테롤 또는 그 전구체와 대사산물의 비정상적인 양, 비정상적인 세포 내 지방화 또는 산화상태 등이 합쳐져서 발생하며, 일차적으로는 연령, 대사성 스트레스 및 유전자 다형성을 비롯한 여러 요인에 의해 발생한다. Cholesterol distress는 부분적으로 Aβ의 생성을 포함하는 메카니즘을 통해 APP 주도 적응반응을 활성화시키게 된다. APP의 적응 반응이 불충분하면 콜레스테롤부조화로 인해 세포기능장애를 야기할 수 있으며, 세포기능장애는 주로 염증에 의해 유발되는 메카니즘을 통해 콜레스테롤 조절에 영향을 줄 수 있다. 알츠하이머의 발병과정은 세포기능장애 이후에 일어나는데, 시냅스 붕괴, 수지상 세포의 소실 및 신경세포 파괴로 이어지면서 치매 및 사망에 이르게 된다. Aβ oligomer와 Aβ plaque는 APP로부터 시작되어 만성 콜레스테롤부조화에 이르는 과정에서 과도한 방어반응이 있을 때 형성된다. 세포기능장애가 이미 진행 중인 뇌에서 즉, 알츠하이머로 이어지는 발병과정 내에서 과량의 Aβ는 이미 취약한 상태의 뉴런에 영향을 미치게 되고, 이어서 염증반응 유도, 산화적 손상 확산, 타우의 과인산화 및 응집을 일으키게 한다. Aβ의 혈관침착은 이 단계에서 두드러지게 나타나 뇌의 아밀로이드 혈관병증과 미세출혈에 기여하여 발병과정을 과도하게 악화시킨다(그림 5).
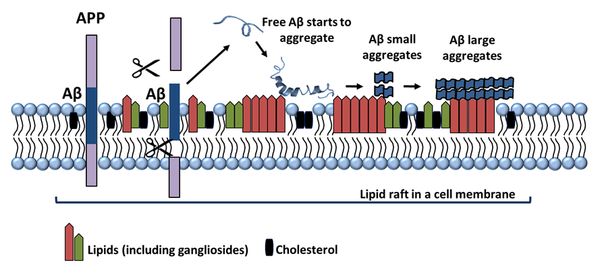
한편 콜레스테롤은 in vitro와 in vivo에서 단백질과 여러 형태의 지질로 조합을 이루어 다양한 형태의 Aβ 응집체의 변이를 유도하고, Aβ는 cholesterol, gangliosides 및 phospholipids과 같은 지질 뗏목성분(lipid raft components)과 상호 작용하여 세포막에 응집한 후 채널 모양의 구멍(channel-like pores)을 형성함으로써 세포막을 파괴할 수 있다. 세포막에서 이러한 Aβ와 지질과의 상호작용이 AD에서 신경독성 캐스케이드를 유발할 수 있으며, 따라서 특정 지질, 지질 조합 및 APOE의 역할이 Aβ 처리, 제거 및 응집에 중요하다.
알츠하이머에서 콜레스테롤의 분자 역할은 분명하지 않지만 실제로 콜레스테롤 수치의 상승은 알츠하이머의 위험 요소이며, 콜레스테롤이 많은 식이는 세포내부의 Aβ 축적을 촉진하고 뇌의 ABB(Aβ burden)를 증가시킨다. 따라서 이러한 혈중 콜레스테롤 상승과 알츠하이머의 연관성은 콜레스테롤 저하 약물이 환자에게 도움이 될 가능성을 높였으며, 일부 세포 및 동물 모델 연구는 콜레스테롤 저하제가 뇌 세포에서 Aβ의 수치를 감소시킬 수 있다고 보고하였다. 그러나 AD의 치료에서 지질강하제의 역할에 대한 명확한 결론을 내리기 위해서는 보다 더 많은 연구가 필요하다(그림 6).
흡연 및 과음이 알츠하이머를 유발한다.
WHO와 알츠하이머질병협회(Alzheimer’s Disease International, ADI)는 흡연자는 비흡연자보다 알츠하이머 발생 위험이 45% 높았으며, 전 세계의 알츠하이머 환자 중 14%가 잠재적으로 흡연에 기인한다고 보고하였다. 또한 현재 흡연하는 사람은 비흡연자보다 2년 후 알츠하이머에 걸릴 확률이 3배 높다고 밝혔다.
흡연은 알츠하이머의 중요하고 실질적인 위험 요소이다. 담배업계는 흡연이 알츠하이머를 보호한다는 입장을 뒷받침하는 연구를 적극적으로 지원해 왔으며, 그러나 지난 20년간 연구는 흡연과 알츠하이머의 관련성에 대한 상반된 결과를 보고했다. 세계보건기구(WHO)가 검토한 바에 따르면 흡연이 알츠하이머 발병에 강한 연관이 있는 것으로 밝혀졌으며, 흡연이 많을수록 알츠하이머 발병 위험도가 높다고 밝혔다. WHO와 알츠하이머질병협회(Alzheimer’s Disease International, ADI)는 흡연자는 비흡연자보다 알츠하이머 발생 위험이 45% 높았으며, 전 세계의 알츠하이머 환자 중 14%가 잠재적으로 흡연에 기인한다고 보고하였다. 또한 현재 흡연하는 사람은 비흡연자보다 2년 후 알츠하이머에 걸릴 확률이 3배 높다고 밝혔다.
또한 WHO는 간접흡연(담배연기)도 알츠하이머의 위험을 증가시킬 수 있다고 보고하였으며, 흡연과 관련된 뇌 산화 스트레스는 알츠하이머 병리 생리학을 촉진시키고 알츠하이머의 위험을 증가시키는 잠재적 메카니즘이라고 밝혔다. 중년의 흡연은 알츠하이머 관련 병리학적 Aβ 축적, tau 과인산화 및 잠재적인 경미한 뇌혈관 장애를 시작함으로써 전임상기간을 단축시킬 수 있으며 또한 뇌 아밀로이드 혈관병증을 현저히 젊은 연령으로 낮춤으로써 알츠하이머에 대한 위험도가 유의하게 증가했음을 보여주었다.
흡연과 알츠하이머의 상관관계에 대해서는 흡연에 의해 알츠하이머의 위험이 증가하지만 한편 흡연과 관련된 알츠하이머의 위험이 없다는 결과는 APOE4 대립 유전자가 없는 경우에만 국한된다고 보고하였다. 또한 폭음과 과음은 인지장애 확률을 1.7배 높이는 것으로 알려졌으며, 중년부터 음주가 잦으면 노년기 인지장애 확률이 2.6배 증가하며, 습관적 음주는 알코올성 치매의 원인이 되는 것으로 밝혀졌다.
알츠하이머에 도움이 될 수 있는 안전한 식생활
건강에 좋은 음식을 먹는 습관이 알츠하이머에 도움이 될 수 있으며 안전한 식생활은 다음과 같다.
(a) 식사는 천천히 꼭꼭 씹어 조금씩 자주 먹도록 한다.
(b) 과도한 음식 섭취를 피한다.
(c) 건강식, 일식 또는 지중해 식단을 먹는다.
(d) 좋은 지방(오메가 3, DHA, EPA, 리놀렌산)이 많이 들어 있는 해산물 등 푸른 생선, 견과류, 아마 씨, 올리브유 등을 섭
취하고, 나쁜 지방(오메가 6, 동물성 포화지방, 경화 식물성 기름, 트랜스 지방산, 야채 기름, 옥수수 기름)이 많은 육류,
버터(풀을 먹고 자란 소에서 얻은 버터 제외), 치즈, 마가린, 마요네즈, 가공식품 등을 피한다.
(e) 비타민을 골고루 적절히 섭취한다.
(f) 항산화 식품(자두, 노니, 블루베리, 시금치, 케일, 브로콜리, 근대 등의 색이 짙은 과일과 채소)을 섭취한다.
(g) 지나친 카페인 섭취를 피한다.
(h) 물을 충분히 마신다.
알츠하이머 환자의 일상생활동작 검사
알츠하이머 환자로 진단하기 전에 일상에서 생활능력 수준을 평가한다. 즉, 세수하기, 양치질하기, 식사하기, 옷 갈아입기, 대소변 가리기 등의 기본적인 일상생활과 반찬 만들기, 전화 받기, 잔돈 챙기기 등과 같은 좀 더 복잡한 일상생활 동작에 대해 평가하고 이러한 검사는 진단을 위한 평가에 이용될 뿐만 아니라, 향후 환자 치료에도 도움이 되는 기본정보로 기록된다. 만약, AD로 진단받기 이전에 SCD 또는 MCI 단계에서 어떤 특징을 가진 환자가 AD로 진행될 위험이 큰지 미리 예측할 수 있다면 조기 진단과 치료에 큰 도움이 될 것이다. 알츠하이머를 예방하기 위해서 무엇보다 우선되어야 할 일은 뇌신경세포를 강화시키는 일이며, 평소 뇌의 대화시스템인 글리코영양소를 충분히 섭취하여 뇌를 보호하고 뇌의 시스템이 잘 작동 되게 하여 Aβ(β-amyloid)를 잘 배출시키고 시냅스를 강하게 유지시키면 Aβ plaque가 형성되더라도 시냅스를 파괴하지 못한다.

