인간게놈프로젝트가 완성된 이후에 인간의 질병을 이해하는 데 있어서 괄목한 발전을 기대하였습니다. 1,000개 가까운 유전자가 인간의 질병과 관계있음이 밝혀졌고 그중에 97%정도는 한 개의 기능이상유전자가 관여하는 단일 유전자의 변형에 의하여 질병이 발생한다고 합니다. 예를 들면 갈락토스혈증(galacosemia)은 galactos-1-phosphate uridyltransferase (GALT) 라는 효소의 결핍이 있는 열성 유전되는 희귀질환으로 혈액에 갈락토오스가 축척되면서 정신 지체가 나타나는 병입니다. 또 다른 예를 들면 페닐케톤요증(phenylketonuria)은 phenylalanine hydroxylase에 결함이 있어서 혈액 내에 페닐알라닌이 축척되면서 심하게 신경학적 손상의 위험을 증가시키는 병입니다. 전자의 경우 갈락토오스가 없는 음식을 주고 후자의 경우는 페닐알라닌의 공급을 중단하고 그 대신 타이로신(tyrosine)이 있는 음식을 공급해주면 영양학적으로 해결할 수 있는 질병입니다.
이와는 대조적으로 서구화된 사회에서 늘어나고 있는 암, 비만, 당뇨병과 심혈관계 질환 등은 단일 유전자(monogenic)의 변이에 의하여 생기는 병이 아니고 다유전자성(polygenic) 변이에 의하여 생기는 복잡한 질병입니다. 예를 들면 2000년에 Segal 등이 메타 분석한 결과를 보면 22가지의 종양에 있어서 종양이 발생될 때 어떤 것도 단일유전자 변이에 의한 것은 없었습니다. 그러므로 음식을 통하여 이러한 질병을 예방하려면 복잡하고 애매하기 때문에 단일 영양소뿐만 아니라 음식 같은 복잡한 영양소의 혼합물들이 상호작용하여 생물학적 기능을 조절 할 것이라 추정할 수 있습니다.
영양유전체학 (Nutrigenomics)
이전에 언급한 것처럼, 영양유전체학은 강력하고 흥미진진한 방법으로 영양이 건강에 미치는 효과를 밝히는 학문입니다. 건강관리에 있어서 영양에 대한 이러한 접근방법과 역할의 잠재력은 매우 다양합니다. 하지만 성공적으로 영양유전체학이 이루어지려면 최근의 영양에 대한 광범위한 지식과 정보가 요구됩니다. 유전학적으로 특정되지 않은 인구집단에서 단순한 역학 조사만으로 영양과 만성질환에 대한 관계를 밝히는 것은 불가능 합니다. 완전한 유전체의 배열을 알아내기 이전에는, 질병의 발생에 기여하는 음식의 역할을 찾기 위하여 시행하는 통합적인 물질대사에 대한 연구방법은 현실적으로 불가능했습니다. 그러므로 역학조사를 포함한 실험적 연구의 대부분은 다양한 질병을 이해하는데 흔하고 특징적인 생체지표를 이용해야 합니다. 예를 들면 심혈관계 질환과 그에 따른 질병들에 대한 연구에서는 전통적인 생체지표로 혈중 콜레스테롤, 중성지방 혹은 C-반응단백 등을 이용할 수 있습니다. 이러한 연구가 질병상태에 대한 우리들의 지식의 타당성과 정확도를 지속적으로 개선시켰습니다. 그러나 고유한 작용기전의 인식 능력의 감별과 혹은 말기가 아닌 조기에 건강상태를 좀 더 정확히 표시할 수 있는 생체지표는 그리 많지 않습니다. 영양유전체학적 기술은 이전에 알지 못하고 예측하지 못했던 분자생물학적인 종착점을 미리 알아냄으로서 이러한 협소한 시야에서 벗어 날 수 있게 해줍니다.
식물성 스테롤(Plant sterols) 과 시토스테롤혈증 (Sitosterolemia)
장내에서 스테롤의 흡수를 조절과 시토스테롤혈증에 있는 유전질환에 대한 분자학적 근거의 기전을 동시에 밝히는 연구가 많이 이루어 졌습니다. 콜레스테롤과 구조적으로 비슷한 식물성 스테롤이 정상적으로는 무시할 만큼의 양이 정상적으로 흡수 되나, 시토스테롤혈증에서는 식물성 스테롤이 고농도로 흡수되는 것에 대한 기전은 이러한 연구가 이루어지기 전까지는 알지 못하였습니다. 콜레스테롤이 HDL로 잘 이동하지 못함으로서 고지질혈증을 일으키게 되는데 유전자의 변이에 의하여 장내세포의 첨단부 표면에서 새롭게 흡수된 동물성과 식물성 스테롤의 선택적으로 조절되는 이동이 잘못 되어서 생기는 병입니다.
긴사슬 불포화지방산(Long-chain polyunsaturated fatty acid, LC-PUFA)과 암의 발생
현재까지 긴사슬 불포화지방산의 섭취가 인간에 미치는 영향이 영양유전체학적 관점에서 분자생물학적 기전은 실험적으로 밝혀져 있지 않았습니다. 그러나 동물실험에서는 긴사슬 불포화지방산이 건강한 세포와 암세포에서 조절하는 기전이 밝혀졌습니다.
긴사슬 불포화지방산의 섭취가 성장, 신경의 발달, 체중감소, 지방량의 변화, 생식, 선천성 및 후천성 면역, 바이러스, 세균 및 기생충 감염의 생리적인 변화에 좋은 영향을 준다는 것이 관찰 되었습니다. 그리고 암, 동맥경화, 뇌졸중, 관절염, 당뇨병, 골다공증 및 신경퇴행성 질환, 염증 및 피부질환과 같은 만성 질환의 발병율과 중중도에 영향을 준다는 것을 알 게 되었습니다.
긴사슬 불포화지방산은 peroxisome proliferator activated receptors, hepatic nuclear factor-4, sterol regulatory expressed binding protein(SREBP), liver-X-receptor α, NFkβ같은 매우 중요한 전사인자(transcriptional factors)와 리간드(ligands)를 형성함으로서 여러 가지 다양한 이질적인 기전을 통하여 건강에 영향을 미치게 됩니다. 긴사슬 불포화지방산이 지방대사의 변화와 인지질, 중성지방 및 콜레스테롤 에스테르(Cholesterol ester, CEs) 같은 몇 가지 지방의 구조 변경에 관여 합니다. 역학 연구에 따르면 긴사슬 불포화지방산은 건강에 대하여 광범위한 영향을 주는 것으로 알려져 있습니다.
암의 발생은 유전자 발현에 있어서 여러 가지 다양한 단계의 변화에 의하여 발생 됩니다. 단백질과 대사산물의 기능 이상이 작동되면서 시작되게 됩니다. 암이 발생되는데 세포학적인 관점도 중요하지만 긴사슬 불포화지방산 같은 음식에 의한 요소가 암의 발생을 조절하고 암의 성장을 이해하는데 또한 중요한 역할을 하게 됩니다. 오메가 3가 풍부한 생선기름이 대장암의 성장을 억제하는 것이 밝혀졌습니다. 최근의 영양유전체학적 기술이 생물정보학(biofinformatics)과 결합되어 긴사슬 불포화지방산의 신호체계의 복잡성이 밝혀지고 있습니다(그림 1 참조). 긴사슬 불포화지방산은 몇 가지 전사인자, 세포주기 조절 유전자, RNA 전사인자, 프로스타글란딘 합성 및 유도된 산화질소 생성효소 (inducible nitric oxide synthase)및 관계있는 염증성유전자의 기능을 중재합니다. 그러나 긴사슬 불포화지방산이 이러한 생물학적 과정을 조절함에 있어서 직, 간접적으로 어느 정도 영향을 주는 지는 아직 잘 모르고 있습니다.
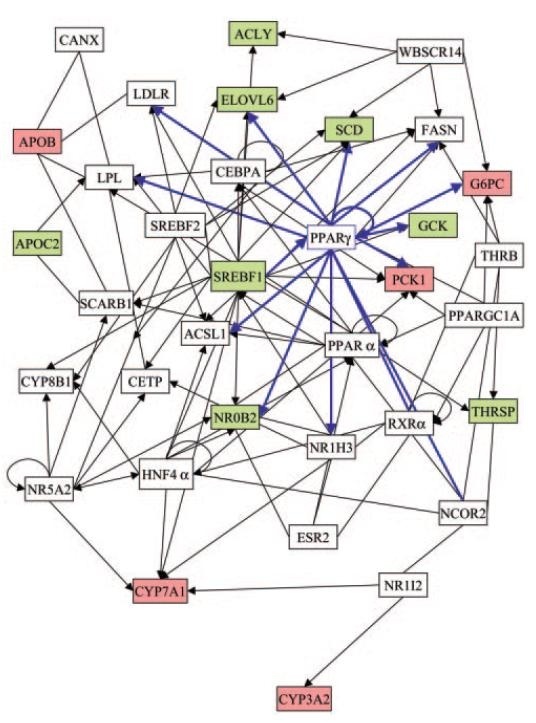 그림 1. 긴사슬 불포화지방산을 섭취후의 변화되는 생물학적인 거미망
그림 1. 긴사슬 불포화지방산을 섭취후의 변화되는 생물학적인 거미망
긴사슬 불포화지방산의 작용은 PPAR과 SREBP에 같은 전사인자를 통하여 발현된다. 이러한 전사인자는 서로 다른 기전으로 직·간접적으로 발현된다. 파란색은 PEAR-γ와 다른 유전자사이의 상호작용을 표시한다. 녹색은 하향조절(down-regulation)을 표시하고 적색은 상향조절(up-regulation)을 표시한다. 백색은 주어진 유전자와 관련이 없음을 표시한다.
Rosiglitazone과 2형 당뇨병
최근 대사체에 대한 검사기술이 획기적으로 발전되면서 지금 까지 발견할 수 없었던 조직의 독성에 대한 생체지표를 발견할 수 있게 되었습니다. 미세한 변화까지도 측정할 수 있는 기술이 개발되면서 당뇨병에서 대사의 변화를 찾아내서 부작용을 최소화 할 수 있는 단계에 이르렀습니다. 동물실험에서 2형 당뇨병에서 흔히 사용하는 rosiglitazone을 투여 시에 간, 지방세포 및 심장조직에서 지방대사의 변화를 측정할 수 있는, 앞에서 언급한 조직세포에서는 지방산의 합성이 매우 증가하였으나 혈장에서 측정한 지질의 양은 증가하지 않았습니다. 그러므로 지금까지 rosiglitazone이 지방의 새로운 합성을 감소시킨다고 알려진 사실은 기존의 표준 생체지표가 진실을 반영하지 못한다는 것입니다. 실제는 국소적으로는 지방이 합성이 증가되며 조직 내에 출/입 되는 것을 조절하는 과정이 변형되기 때문에 장기적으로 rosiglitazone치료를 하는 경우에 부작용이 감춰질 수도 있습니다. 음식의 섭취 후 일어나는 대사체의 변화를 영양과 관련된 질병을 찾기 위하여 검사하는 특정 생체지표만을 통하여 알 수 있는 것은 쉽지 않으며, rosiglitazone 같은 약물복합제보다 영양소가 대사체의 변화에는 더 미미한 변화를 일으킵니다.
영양유전학(Nutrigenetics)
영양유전학(nutrigenetics)이란 인체의 체질에 따라 섭취한 음식성분이 어떻게 반응하는가를 연구하는 학문 분야입니다. 모든 사람의 유전자가 동일하다면 음식에 대한 반응이 똑 같이 나오겠지만, 인간게놈프로젝트를 통하여 완전하게 염기서열을 파악하였지만 단일염기다형성(SNP, single nucleotide polymorphism)에 의하여 개개인의 표현형의 차이를 결정한다는 것이 알려져 있습니다. 심혈관계질환 및 당뇨병 같은 많은 만성질환에서의 치료에 대한 반응도 이러한 원칙이 적용된다는 뜻입니다. 단일염기다형성을 분석하는 것은 인간의 건강과 질병에 있어서 영양의 역할을 연구하는데 강력한 분자학적 도구로 사용될 수 있습니다. 그 결과는 임상적, 대사학적 및 역학적인 연구를 통하여 이상적인 음식을 찾아내는데 무한한 가능성을 제시해 줄 수 있습니다.
이와 같이 영양학적인 관점에서 역학적 연구는 개인적 차이가 있기 때문에 획일적이고 균일한 표준을 정할 수 없다는 것은 매우 중요한 사실입니다. 그럼에도 불구하고 유전자 변이와 식사요법 사이의 관계를 인슐린 저항성, 2형 당뇨병 및 심혈관계 질환과 연결하여 어떻게 유전적 요소가 음식에 의하여 질병이 예방되는지에 대한 많은 연구가 진행 되었습니다.
심장관상동맥 질환
심장관상동맥 질환은 서구에서는 가장 흔한 질병 중에 하나이며, 미국에서는 사망하는 사람 5명중에 1명의 원인이 됩니다. 역학연구에 따르면 지방과 심장관상동맥 질환과는 분명한 인과 관계가 있습니다. 국제 지질 교육 프로그램(The National Cholesterol Education Program)에서도 저밀도 지방(LDL, low density lipoprotein)과 고밀도 지방(HDL, high density lipoprotein)같은 지단백(lipoprotein)의 조절을 심장관상동맥 질환의 치료에 중요한 목표점으로 고려하고 있습니다. 여러 가지 복합체가 존재하는데 구성성분에 따라 밀도의 차이가 있어서 다음과 같이 구분합니다.: chylomicron(high lipid to protein ratio, 무게%에서 TGs가 가장 높음), VLDL(very low density lipoprotein, 무게%에서 TGs가 2번째로 높음), IDL(intermediate density lipoprotein), LDL(무게%에서 cholesterol ester가 가장 높음) 및 HDL(high protein to lipid ratio). 임상적으로 보면 심장관상동맥 질환의 예방을 위한 방법은 지질의 농도를 낮추는데 있습니다. 일차적인 치료는 생활습관 변화, 즉 각 개인의 음식, 육체적 활동의 변화를 시켜주고, 추가로 가능하다면 금연 및 체중감소를 유도해 줍니다. 두 번째로는 statin 약물을 처방합니다. statin은 간에서 3-hydroxy-3-methylglutaryl CoA 환원효소(HMG CoA reductase)를 억제하여 결국 순환계 내의 콜레스테롤을 감소시켜줍니다. 그러나 개인차이가 있기 때문에 이러한 치료방법들이 반듯이 목표한 정도까지 도달하지 못한다는 것입니다. 이러한 다양한 반응의 차이는 유전적인 차이가 있기 때문입니다. 즉 유전자의 차이가 심장관상동맥 질환의 시작이나 예방에 결정적인 역할을 한다는 뜻입니다.
cholesterol ester transfer protein (CETP), lipoprotein lipase(LPL), hepatic triglyceride lipase(HL), LDL-receptor, apolipoprotein E(APOE), apolipoprotein A1(APOA1), ATP binding cassette transporter A1(ABCA1) 및 lecithin-cholesterol acyltransferase(LCAT)와 같은 유전자의 다양한 변이는 심장관상동맥 질환을 일으키는 각 개인의 감수성을 변화 시킵니다. 특히 APOA1 과 LPL에서 다형성(polymorphism)은 식사요법에 매우 민감하며 심장관상동맥 질환의 발현을 조절할 수 있습니다.
● Apolipoprotein A1 (APOA1)
HDL은 심장관상동맥 질환의 예방에 가장 중요한 역할을 하는데, 주로 말초 조직에서 간으로 콜레스테롤을 배달하여 담즙으로 내보냅니다. APOA1은 혈장 HDL의 주된 구성 요소이며, 콜레스테롤을 ABCA1에서 HDL입자로 전송하는 역할을 하는 것으로 알려져 있습니다. 최근의 연구에 따르면 불포화지방산(PUFA, polyunsaturated fatty acid)같은 음식물의 요소가 HDL농도에 변화를 일으킵니다. APOA1에 대한 유전자의 다형성은 섭취한 음식물속의 PUFA에 대한 반응을 다르게 합니다. 또한 남녀의 차이도 존재한다고 하였습니다. 남자에서는 APOA1에 대한 유전자의 다형성에 상관없이 PUFA소모량과 HDL 농도사이에는 연관성이 없었습니다.
● Lipoprotein lipase (LPL)
LPL은 순환하는 chymomicron과 VLDL 입자에 존재하는 TG의 가수분해를 촉매하여 비에스테르형 지방산(NEFA, nonesterified fatty acid)과 2-monoacylglycerol 만들어서 조직에서 이용할 수 있게 해줍니다. LPL에 기능이상이 생기면 동맥경화, chylomicron혈증, 비만, 알츠하이머병, 지질이상혈증과 동반된 당뇨병 및 인슐린 저항성 등과 연관성이 있습니다. 결론적으로 LPL은 인체 내에서 지질대사에 있어서 총체적인 조절을 하는 것을 알 수 있습니다.
인슐린 저항성과 2형 당뇨병
2형 당뇨병은 인슐린의 분비가 불충분 하거나 정상적인 작용을 하지 못해서 생기는 병으로 고지혈증, 이상지질혈증 및 탄수화물, 단백질 및 지질대사에 이상을 초래하는 병입니다. 서구화된 사회에서 육체적 활동이 적어지고 운동을 하지 않으면서 과량의 음식을 섭취했을 때 잘 올 수 있는 질병이며, 그 외에도 환경오염과 유전적요소가 원인이 될 수 있습니다. 우리나라도 지난 30년간 10-20배 정도로 당뇨병의 유병률이 증가 되었습니다. SREBP(Sterol response element binding protein)-1a 및 1c에서 변이가 되면 지방산합성에서 매우 중요한 역할의 변화가 오게 됩니다. 동물실험에서 보면 간과 지방세포에서 SREBP-1c 유전자의 과도한 발현은 전사인자에 이상을 초래하여 당뇨의 발생에 중요한 역할을 합니다. 이유는 TG와 CE(cholesterol ester)가 증가되어 지방간이 만들어 집니다. 그 결과 고중성지방혈증, 중중의 인슐린 저항성, 2형 당뇨병이 생기게 됩니다. SREBP-1c의 발현은 음식물에 예민하기 때문에 식사요법에 중요한 목표점이 될 수 있습니다. 즉 이형성증이 분자생물학적인 조절능력의 변화 및 식사요법에 대한 감수성의 변화까지 초래할 수 있습니다.
PPARS(Peroxisome proliferator-activated receptors)는 fibrates, thiazolinediones(TZDs), 지방산 및 지방산 유도체의 세포내 반응을 매개하는 중요한 전사인자입니다. α, β/δ 및 γ 의 3가지 종류의 PPAR가 있으며 지방산 분해, 지방세포 분화, 및 상처치유에 관여하는 것으로 알려져 있습니다. 제약업계에서는 PPAR-γ에 관심이 많은데. 그 이유는 이것이 활성화 되면 지방세포의 형성과 지방산의 이송을 통한 중성지방의 저장 및 당신생의 조절에 중요한 역할을 하기 때문입니다. TZDs에 의하여 PPAR-γ이 활성화 되면 순환하는 지방산을 지방세포에 모음으로서 결국 인슐린 감수성을 증가 시킵니다.
우리가 먹는 음식이 생존에 필수적이 요소라는 것은 여러 면에서 분명하게 입증되었습니다. 음식이 질병을 일으킬 수도 있고 치유시킬 수도 있습니다. 바꿔 말하면 살아가는 방식의 차이에 따라 질병유전자의 발현이 결정될 수 있기 때문에 과거에 많지 않았던 고혈압, 2형 당뇨병, 심혈관계 질환, 암 등의 병들은 음식을 포함한 생활습관을 바꿔줌으로서 근본적인 예방과 치료가 될 수 있습니다. 첨단 과학의 발달을 이용하여 좀 더 구체적으로 원인을 규명할 수 있으며 나가가서 많은 난치병들에 대한 치료방법을 제시할 수 있는 희망이 될 것으로 사료됩니다. “음식물을 너의 의사나 약으로 삼아라. 음식물로 고치지 못하는 병은 의사도 못 고친다”라는 희랍의 의성 히포크라테스의 말씀을 다시 한 번 생각해 봐야 할 것 같습니다.

