 현대에 들어와 먹거리의 종류와 그 수가 매우 늘어난 것은 사실이다. 그러나 그 먹거리 자체의 영양함유량은 과거에 비해 갈수록 현저히 떨어지고 있다. 50년 전에는 비타민A의 일일필요량을 복숭아 2개에서 섭취할 수 있었다면, 현재는 그 26배인 복숭아 52개를 먹어야 일일필요량을 충족시킬 수 있다.
현대에 들어와 먹거리의 종류와 그 수가 매우 늘어난 것은 사실이다. 그러나 그 먹거리 자체의 영양함유량은 과거에 비해 갈수록 현저히 떨어지고 있다. 50년 전에는 비타민A의 일일필요량을 복숭아 2개에서 섭취할 수 있었다면, 현재는 그 26배인 복숭아 52개를 먹어야 일일필요량을 충족시킬 수 있다.
그 이유로는 지나친 비료와 농약 등의 사용, 휴경 없는 경작으로 인한 토양의 황폐화, 지나친 조기수확, 원거리 운송, 가공식품의 발달 등을 꼽을 수 있다. 그러나 사실상 적절한 영양소의 공급은 간과해서는 안될 중요한 문제이다.
18세기 후반 비타민C 부족으로 인한 괴혈병을 신선한 과일을 공급함으로 해서 치료할 수 있다는 역사적인 사실의 발견 이후로 점차 중요한 문제로 부각되고 자리 잡았다.

1977년 미국 상원에서 맥거번 보고서가 발표된 이래로 미국에서부터 이러한 영양요법의 교육과 중요성은 더욱이 커져왔다. 그와 더불어 환자의 치료에 있어 영양을 포함한 대체요법이 점차 그 비중을 늘려가고 있는 상황이다.

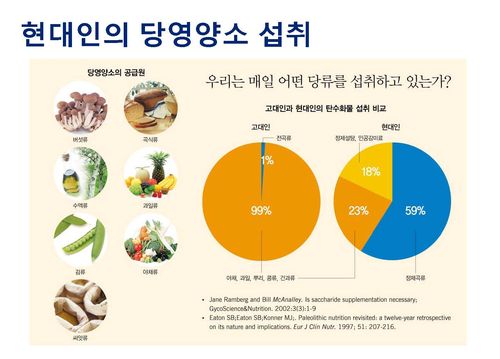
현대인들에게 있어서 탄수화물, 단백질, 지방 외 비타민, 미네랄은 필수영양소로써 규정되어 상당히 오랫동안 5대 영양소로 알려져 왔다. 여기에 2000년대 이후 식물내재 영양소와 물의 중요성이 커지면서 1990년대에 알려진 세포에 필요한 8대 당영양소 역시 단순 에너지원이 아닌 세포의 기능에 깊이 관여하는 중요한 기본 영양소로 추가되었다.
실제 현대인들에게 부족한 영양소 종류에는 앞서 언급한 기본 영양소가 골고루 포함되지만, 그 중에서도 새로이 추가되어 부각된 당영양소의 섭취 부족이 가장 심각한 수준이다. 결과적으로 당영양소로 이루어진 세포의 당사슬의 수가 급격히 감소하여 관련 질환의 증가로 이어진 것이다.
이러한 질환의 증가는, 현재 성인의 삶의 질을 떨어뜨려 심각한 문제를 야기하고 있긴 하지만 더욱이 주목해야 할 문제는 아이들, 즉 우리의 후손들에게까지 해당 문제가 이어지며 그 정도가 심각해진다는 것이다.
실제 오랫동안 소아 환자를 보아온 필자의 입장에서 과거와는 달리 아이들의 질환 또한 성인의 질환과 유사해지고 있으며 아주 이른 나이부터 증상이 시작되는 것을 보아왔다.
즉, 세대를 잇는 당영양소 결핍으로 인한 조기 질환의 증가가 출생률 감소와 아울러 우리아이들에게, 그리고 사회에 중요한 문제가 될 수도 있는 상태인 것이다.
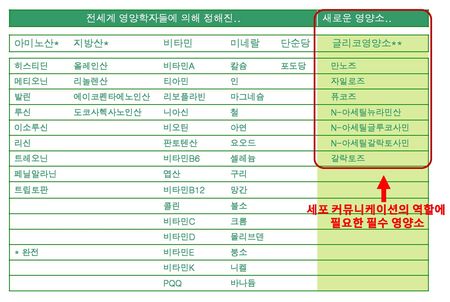
소아에 있어서 성장과 발달은 굉장히 중요한데, 이러한 성장은 태내에서부터 시작되어 꾸준히 이어진다. 이러한 성장에 영향을 미치는 요소로는 유전, 환경, 문화, 건강상태, 가족, 양육태도, 영양 등이 있는데 이 중 영양이 가장 중요한 요소이다. 인체 필수 영양소는 구체적으로 다음의 표에 기재되어있는 것과 같다(표1).
그 중 앞서 언급했듯이 20세기에 새로이 대두된 당영양소가 핵심적인 역할을 하고 있다. 당영양소가 부족할 때 여러 가지 면역질환, 학습장애, 주의집중장애 등의 질환과 아울러 태내에서 선천성 대사 장애를 일으키는데 이를 ‘선천성 당화 결함’이라 한다.
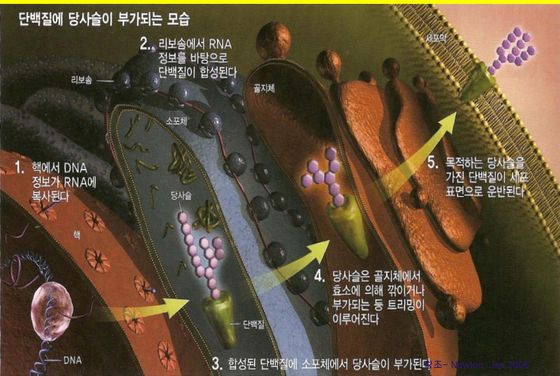
이에 당화 과정과, 태내에서부터 시작되는 당화결함으로 인한 질환 그리고 그 대책에 대해서 논의해 보고자 한다. 단백질의 당화과정은 다당류 복합체가 post-translation linkage를 통해서 단백질에 부착되는 것이다.
당단백질의 역할은 단백질의 stability, solubility and polarity에 관여하며 생물학적 과정들인 성장, 분화, 장기의 성장, 신호전달, 면역반응 그리고 호르몬의 작용에 관여한다.
인간에 있어 이러한 당화과정에 최소한 100개 이상의 단백질이 적어도 40단계의 과정을 거치는데, 결론적으로 전체 유전자의 1~2%가 당화과정에 관여하게 되는 것이다.
이러한 당화과정 결함으로 인한 질환을 pediatric reasearch에서 1980년에 Jaeken 등이 최초로 발표했다. 1999년에는 6개의 CDG1)만이 알려져 있었지만 그 수는 점차 증가하여 현재 50여종으로 늘어났다. CDG라는 것이 알려진지 상당한 시간이 지났지만 그 병태생리는 아직도 상당수 밝혀지지 않았다.

CDG의 발생은 전 세계적 현상이다. 이는 AR로 유전되는데 예외적인 유전방식으로 AD인 EXT1/EXT-2CDG와 X-linked인 MGAT1-CDG가 있다. 그리고 그 발병률은 1:40,000이하로 추정된다.
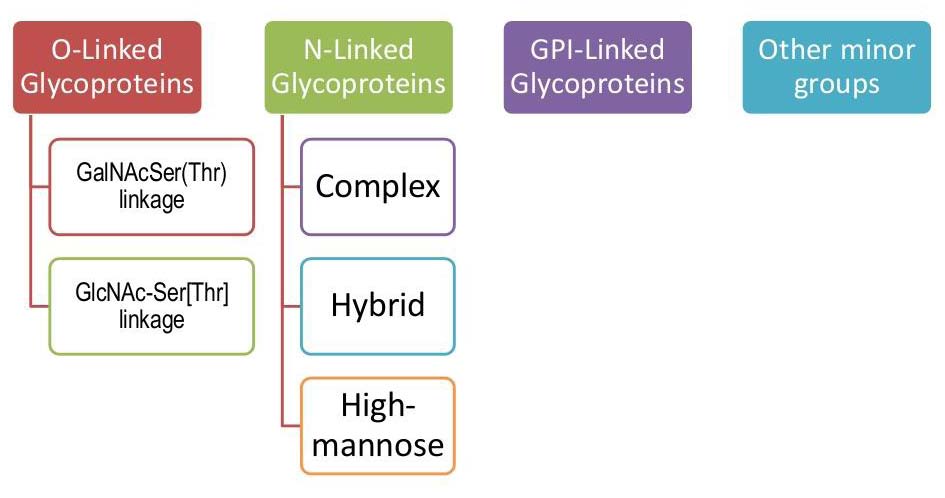
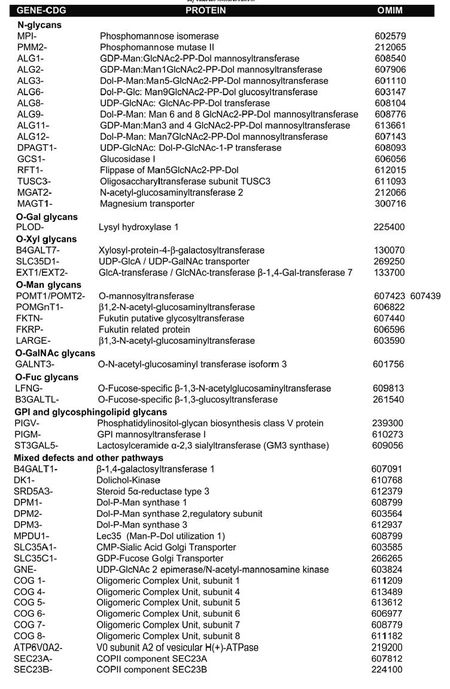
그 중 가장 많이 보고된 예가 CDGIa (PMM2-CDG)이며 그 다음이 CDGIb(PMI-CDG)를 통한 유전이다. 그 분류는 metabolic pathway에 있어 생화학적 결함의 성향과 위치에 따라 결정이 된다. 구체적으로 현재 21개의 type1과 14개의 type2로 나뉘어져 있다.
현재는 2009년 gene defect에 따라서 새로운 명명법이 등장하여 해당 방법으로 명명되고 있다. 당단백질의 분류는 표2.와 같다.
N-glycan의 생성과정은 다음과 같은 단계를 거친다.
1. Formation of nuclesotide-linked sugars
2. Assembly
3. Attachment
4. Processing
(2, 3 : Cytosol & ER, 4 : ER & Golgi에서 각각 일어난다)
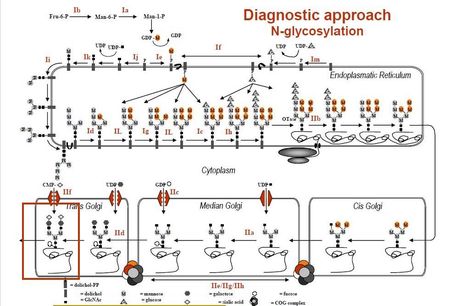
1. CDG-1 : 당사슬의 assembly와 단백질에의 부착의 장애로 인한 질환. 세포질과 소포체에 서 일어난다.
2. CDG-2 : 당사슬의 processing의 장애. ER과 Golgi에서 일어난다.
(※ 기본적인 결함의 발견순서에 따라 소문자로 표시한다.)

1. 다른 기관 침범과 함께 설명할 수 없는 신경학적 증후가 있을 때.
2. 신경학적 증후가 없을 때라도 설명할 수 없는 증후가 있을 때.
CDG질환 그 자체는 의사들에게 있어 상당한 도전일 수 있는데 해당 질환을 간과할 시 종종 영유아기에 심각한 사망률로 이어지기 때문이다. CDG는 전 연령에서 발병하고 모든 기관을 침범하며 그 정도로 다양하므로 기존에 일반적 개념으로는 설명할 수 없는 증상을 보이는 모든 환자에서 고려되어져야 한다. 미토콘드리아증과 같은 다른 대사성질환과는 감별되어져야 한다.
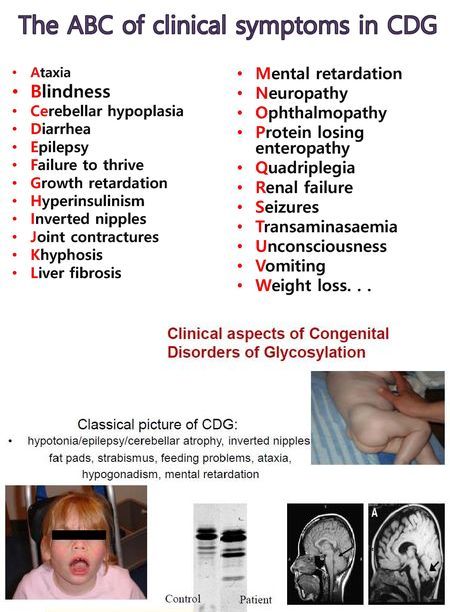
당사슬이 발생, 재생, 그리고 synaptic plasticity에 중요한 역할을 하기 때문에 CDG-Ib를 제외한 대부분의 CDG에서 뇌 증상이 나타난다. CNS, 눈, 소화기계, 피부, 심혈관계, 정형외과적 문제, 호르몬 불균형, 신장질환, 혈액질환, 기타 전신증상 등의 증상이 발생하는 것이다.
검사소견은 다음과 같다.
1. 저콜레스테롤혈증.
2. 저알부민혈증.
3. 인슐린 분비의 부적절한 증가와 더불어 나타나는 저혈당.
4. CDG-Ib에서 보이는 aminotransferase의 활성 증가.
5. CDG-II에서 보이는 aminotransferase 활성의 불균형.
6. 혈청 lysosomal hydrolase의 활성 증가.
7. 응고인자와 응고억제인자인 factor II,Ⅴ,Ⅹ,ⅩI, anti-thrombin III, protein C, S의 변화.
8. T3, T4, and rT3는 대개 subnormal.
환자에 있어서 치료는 가장 중요한 이슈인데 사실 별 특별한 치료가 없으나 일부에서는 치료에 반응을 보이는 경우가 있다. 대개 그 경과는 느린 편이다. 출혈과 혈전의 경향이 증가하므로 반복되는 뇌졸중에는 아스피린을 투여한다. 질환, 마취, 수술 등과 같은 경우에는 탈수를 피해야 하며, 이때 전해질, 혈당, 응고인자들을 조심스럽게 관찰해야한다.
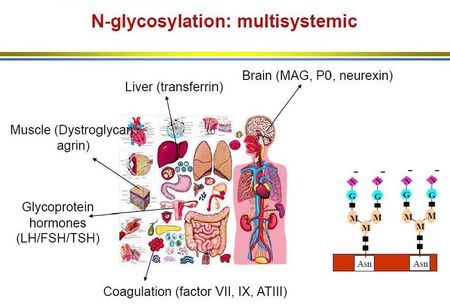
현재 유일하게 효과적 치료가 가능한 type은 MPI-CDG (CDG-Ib)로서 만노스를 매일 경구로 투여하면 현저하게 증상이 개선되는데, 그럼에도 기존의 간섬유화를 호전시키지는 못한다. 그러나 만노스는 거의 부작용이 없이 안전하게 사용될 수 있다.
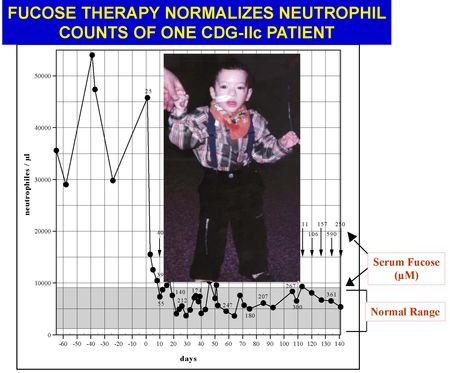
또 다른 type인 CDG-IIc(SLC35c1-CDG, leukocyte adhesion deficiency typeII)에 경구 퓨코스를 투여했을 때 눈에 띌만한 임상적인 증상의 호전을 보였다. 섭취 수일만에 문제가 되었던 호중구 수치가 정상화 된 것이다.
그 외, PIGM-CDG에서 deacetylase inhibitor butyrate를 투여했을 때, 발작이 멈추기도 하였다. 더불어 membrane permanent 유도체인 mannose-1phosphate의 합성이 가장 흔한 N-glycosyaltion 질환인 CDG-Ia의 치료의 시작에 있어 획기적인 방안이 될 수 있음 역시 시사되었다.
선천성 당화결함으로 인한 심각한 신경학적 대사성장애를 가진 신생아에 있어 상당한 숫자의 증후군이 밝혀져 왔다. 이 질환의 증가는 사실 진단기술의 발전과 무관하지 않으며 앞으로도 더욱더 늘어날 것으로 전망된다. 단백질 당화에 관여하는 유전자가 전체의 1~2%에 해당하며, 이는 수백 혹은 그 이상의 당화결함이 발견되어진다는 것을 의미한다.
현재 많은 연구가 기초과학자들과 의사들 사이에서 이루어지고 있다. 이는 유전자 검사를 데이터베이스로 하여 산전 진찰 등을 통해 조기 발견과 이에 따른 적절한 대응을 하려는 노력으로 연결된다. 그리고 수많은 실험을 통해 정확한 진단 뿐 아니라, 치료의 접근에 있어서도 더 큰 발전을 가져올 수 있을 것이다.
우리는 일부환자의 치료에 있어 경구 만노스 및 그 유도체, 혹은 퓨코스의 투여가 성공적이었다는 것을 참고하여, 이러한 당영양소의 더 넓은 응용방안 도출과 발전을 위해 심도 깊은 연구가 필요하다고 생각한다. 그리하여 당영양소의 상용화를 통해 이러한 질환의 성공적인 치료에 기여할 수 있기를 기대한다.

