손안에서 실시간으로 정보가 갱신되고 이것들을 입맛에 맞게 조합한 서비스들이 여러 분야에서 거침없이 통용되는 바야흐로 맞춤화의 시대이다. 정형화된 인체와 조건을 전제로 성립된 “one-size-fits-all” 모델은 이렇게 섬세하게 진화된 시장에 익숙해진 환자군의 수요와 욕구에 맞게 생동하기 힘든 태생적 한계를 가지고 있으며, 전문가들은 건강한 생명 연장을 추구하는 지금은 개인별 맞춤 영양 요법이 적합한 청사진이며 필연적 귀결일 것이라 이야기 하고 있다.
맞춤화, 정밀화의 구현은 유전체학의 태동과 궤를 함께 한다. 2003년 인간유전체 정보가 해독된 이후 13개의 맞춤 영양요법 회사가 출현하였고, 지금은 “Habit, Arivale, InsideTracker, DNAfit, DayTwo, Nutrigenomix” 5개 회사가 유의미한 성장을 이루어 냈다. 영양유전체 회사들의 슬로건은 다음과 같이 대부분 비슷한 맥락을 가지고 있다.
유전체학은 전체 유전체 서열을 밝히는 최초의 범국제적 시도인 인간게놈 프로젝트가 2003년 완성됨과 동시에 급속도로 발전하고 있다. 각 개인의 DNA를 풀어냄으로써 수많은 만성 질환을 줄이고 치유하고 완화시킨다는 이정표는 더욱 가까워졌다. 실질적인 예방 의료 프로그램을 설계하는데 이 정보들을 활용 하는 것이 유전체 의학의 목표이자 유망한 일이 되었다. 지난 13년간 유전체 검사는 실험실을 넘어 임상까지 확장되었고 빠른 속도로 성장 중이다.
최근 유전체학은 폭발적인 도약 지점에 맞닿아 있다. 미국과 세계의 의료 전문가들은 예방 및 치료 전략을 개별 맞춤화하는데 “omics” 혁신의 개념과 원리를 도입하고 있다. 기술과 정보는 기하급수적으로 발전하고 있지만, 임상가들이 그것을 배우고 온전히 이해하여 임상에 통합적용하기까지 소요되는 시간과 자본들은 과제가 되고 있다. 가장 까다로운 숙제 중 하나는 이 새로운 과학적 원칙에 동반되는 용어를 익히고 이것을 기존에 배워왔던 유전학 과정과 조화시키는 일이다.
“유전학”과 “유전체학”이란 용어는 전문가들 사이에서 조차도 적지 않게 혼용되어 오늘날까지 혼란을 초래하고 있다. 유전체학은 유전학의 한 분지이지만, 이 둘 사이의 차이점을 이해하고 건강과 질병에 어떤 영향을 미치는지 이해하는 것은 중요하다. 간단히 말해 유전학은 예측의 영역에서, 유전체학은 반응성, 감수성(susceptibility)의 영역에서 활용된다.
임상적으로 유전학은 소위 표현형이라 일컬어지는 어떤 사람의 발달, 질병위험, 약물 반응에 관한 단일 혹은 일부 유전자에 관한 것이다. 특정 표현형에 배당된 단일 유전자는 한 개의 유전자에 초점이 맞춰져 있기 때문에 보통“monogenic”접근법이라 불린다. 반대로, 유전체학은 genome에 존재하는 모든 유전자의 기능과 상호작용을 연구한다. 유전학에 비해 유전체학은 복잡하고 난해하다. 임상가의 전문적 식견을 기반으로, 새로운 기법의 사용이 특정인의 만성적인 질환의 위험도에 미치는 정도를 파악하기 까지는 시간과 실전경험이 필요하다.
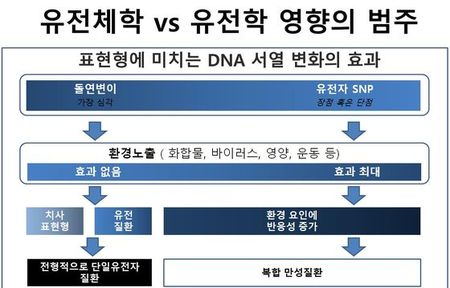
유전학의 고전적 정의는 유전, 즉 형질물림(heredity)에 관한 연구이다. 유기체의 특징과 특성(표현형)이 어떻게 다음세대로 전달되냐는 것이다. 이것은 세포핵에 존재하는 유전자라 불리는 전달의 기본단위인 이중나선 분자구조인 DNA를 통해 일어난다. 초기 유전 연구의 많은 원리와 규칙들이 아우구스티누스회 성직자이자 과학자인 ‘그레고리멘델’의 연구에서 비롯되었다. 1800년대 중반에 이루어진 완두콩을 관찰한 그의 연구는 오늘날 유전학의 기초를 다져놓았다.
돌연변이는 단일 염기의 변화에서 전체 염색체의 변화까지 광범위하게 발생할 수 있으며 이미 알려져 있는 투과도와 유전 양식(penetrance and inheritance pattern)을 따라가고는 한다. 유전질환이 개개인으로는 희귀하지만, 전체 인간 질병의 5%를 차지한다. 생식계열에서 발견되는 희소한 단일 유전자 돌연변이의 영향과 유전적 위험도를 정확하게 예측하기 위해 특정인의 유전 구조나 유전자형(genotype)을 활용할 수 있다. Tay Sachs병, 혈우병, 낭성섬유종증 같은 유전질환이 이 영역에 속한다. 유전자 검사는 특정 질환과 관련된 돌연변이를 확인할 수 있으며 적절한 스크리닝과 치료 계획의 수립을 도와준다. 대부분의 경우 돌연변이의 영향을 선제적으로 완화시키거나 차단할 수 있는 실질적인 방법은 없다.
유전체학은 혜성같이 등장하여 DNA sequencing과 컴퓨터 생물학의 기술적 진보에 힘입어 성장한 20여년의 역사를 가진 최신 학문이다. 모든 질병의 95%는 SNPs라 불리는 일반 유전자 변이와 관련이 있다. 이런 만성 질환들은 유전자 다형성과 환경 변수간의 상호작용에서 비롯되는 다원적, 다인자적 질병이다.
유전자 다형성은 기능적 변화를 초래할 수 있는 DNA nucleotide 서열의 변화를 말한다. DNA서열에서 단일 nucleotide의 치환만으로도 그 위치에 따라 다양한 결과를 야기할 수 있다. 최종 발현되는 단백질의 기능성에 영향을 줄 수도 있고 단백질 합성양을 변화시킬 수도 있지만, 또 전혀 타격이 없을 수도 있다. 덧붙여 유전자 SNP는 표현형에 도움이 될 수도 또 유해할 수도 있다. 유전자 다형성은 유전학과 달리 전형적이고 예상되는 경로를 따라가지 않는다.
유전자 돌연변이와 달리, 단일 유전자 다형성은 일반적으로 표현형에 미미한 영향을 줄 뿐이다. 생화학적 경로나 생물학적 시스템 내의 여러 유전자에 발생하는 SNPs는 추가적인 영향이 더해지며 여타 시스템의 SNPs와도 상호작용할 수 있다.
여기에 추가로 환경적 요소들이 생화학적 대사 경로의 단일 혹은 복수의 유전자 다형성의 영향과 상호작용할 수 있다. 그러므로 만성 질환의 진행과정은 어떤 이의 유전자 SNPs와 환경요인간의 고유한 상호작용을 나타내므로 각 개인의 성, 인종, 지역에 따라 매우 다양할 수 있다. 현 21세기의 다인적, 다원성 만성질환의 유행을 실질적으로 다룰 수 있는 유전적 다양성을 고려하도록 역학적 재정비가 필요하다.
유전체 검사만으로는 질병을 예단할 수 없다.
기존의 대사산물 METABOLIC ANALYSIS, BLOOD SUGAR BIOMARKERS
▷ Disposition index(blood sugar management)
▷ C-peptide-baseline, 30, and 120 minutes(blood sugar management)
▷ Post-meal glucose-30 and 120 minutes(blood sugar levels)
▷ Fasting glucose(blood sugar level)
▷ Blood sugar management gene variants
CHOLESTEROL BIOMARKERS
▷ Total Cholesterol
▷ LDL Cholesterol
▷ HDL Cholesterol
▷ Cholesterol balance gene variants
TRIGLYCERIDE BIOMARKERS
▷ Fasting triglycerides
▷ Post-meal triglycerides-30 and 120 minutes
▷ Triglyceride balance gene variant
SELF-REPORTED BIOMARKERS
▷ Core waist measurement
▷ Activity level
▷ Sex
▷ Height
▷ Blood pressure
▷ Age
진단에서 예후추정까지
“Quantified Self”를 스스로 점검하고 확인하여 유전체 검사 결과와 함께 분석할 수 있어야 현 건강 상태를 개선하고 질환을 예방하는 진정한 개인별 맞춤 영양요법을 계획 할 수 있다. 2017년 8월 J. Bland는 interpreting your genetics의 강의에서, 현재 질병에 중점을 둔 Monogenic disorders에 대한 genetic counselor의 서비스는 가능하지만 유전체와 환경적 변수를 균형 있게 분석하고 반영할 수 있는 polygenic counselor는 미국 시장에서 아직 찾아보지 못했다고 언급하였다. 다원적 요인으로 얽힌 질병의 해결은 통합기능의학적 패러다임과 방향에 이상적으로 부합하는 만큼, 한국 통합기능의학 의료진들에게도 열심히하여 의미 있는 포지션을 선점할 기회가 남아있다.
인간 genome 연구가 계속 발전함에 따라, 우리는 DNA의 복잡성에 대한 이해가 훨씬 깊어질 것이다. 오늘날 유전학과 유전체학의 경계는 모호해지고 현존하던 유전 패러다임은 변화하고 있다. 많은 과학자들이 이제 유전학과 유전체학을 분리된 영역으로 구분하기 보다는, 높은 투과도를 보이는 생식계열의 단일 유전자 질환이 한쪽 끝이고, 여러 부위의 일반적이고 낮은 투과도의 유전자 변이 혹은 SNPs가 환경요인과 상호작용하여 야기되는 복합질환이 다른 말단에 위치하는 연속된 스펙트럼의 일부로 보고 있다. 이들 사이에는 아직 정의되지 못한 회색 지대가 있다. 유전 연구의 발달은 유전자 돌연변이 발생 기전과 관련해 보다 깊은 통찰을 제공할 것이고 국지적인 세포 환경이 짐작하던 것보다 훨씬 중요한 역할을 할 수 있음을 보여 줄 것이다.

BRCA1돌연변이로 야기되어 유전되는 형태의 유방암을 예로 들어보자. 이것은 규정된 투과도와 유전 양상에 비추어 통상적으로 돌연변이 때문인 것으로 생각해 왔다. 돌연변이 유전자를 가진 여성이 모두 유방암에 걸리는 것이 아니기 때문에 연구가들은 다른 역할을 하는 무언가가 존재하리라 추측해왔다.
BRCA1 유방암 세포 주위의 미세 환경이 유방암 발달에 의미 있는 역할을 할 것이라는 연구 결과가 최근 발표되었다. BRCA1 유전자 돌연변이가 기능상실을 초래한다는 사실은 잘 알려져 있으며 DNA회복 능력의 부족이 암을 발생시키는 주요 기전이라 예측해왔다.
Gorrini등의 쥐를 이용한 최신 연구에서 산화 스트레스 반응 조절을 포함한 추가적인 관련 기전들이 밝혀졌다. 내인적 항산화 연쇄반응의 주조절 유전자인 Nrf2를 포함한 세포 신호가 BRCA1돌연변이에 의해 손상되는 것이 관찰되었다. 동시에 영양 유전체학 연구로, Nfr2의 유전자 SNP로 손상된 항산화 반응이 유방암 위험을 증가시킬 수 있음이 드러났다.
Sulforaphane과 resveratrol을 비롯한 엄청난 생활성 화합물들이 Nrf2유전자 기능을 조절하고, 유전자 SNP Nrf2의 영향을 약화시키며 잠재적으로 유방암 위험을 감소시킬 수 있다. 하지만 이런 유전체적 원리를 BRCA1돌연변이를 가진 해당 여성에게 적용할 수 있는가는 아직 결론내리지는 못했다. 실효적인 유전체 서비스의 공급을 위해서는 유전 정보에 더해 각 개인 고유의 환경적 요소가 반영되어야 한다.
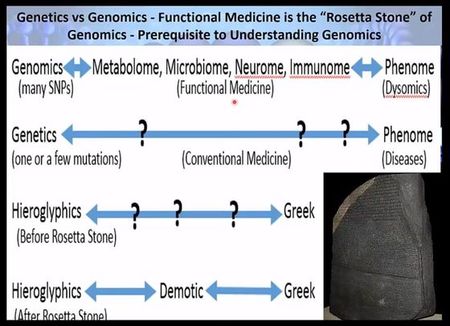
이런 측면에서 Charles Gant, MD는 로제타 스톤이 이집트 상형문자 해독의 징검다리가 되었듯이, 유전체정보를 효과적인 임상 전략으로 연결시킬 수 있는 가교가, 복합적인 네트워킹에 특화되어 있는 통합기능의학일 것이라 주장하고 있다. 정밀 유전체 의학의 미래는 흥미진진할 것이다. 임상 유전체학에 본격적으로 몸담고자 하는 의사들은 그 핵심 개념을 완전히 이해하고 굳건한 기초를 닦아야 한다. 이는 기본 용어의 습득은 물론 오랜 유전학 패러다임과 유전체학의 새로운 영역들의 유사성과 차이점을 인지하는 것으로부터 시작된다. 개별화된 섬세한 접근을 원하고 필요로 하는 환자 수요는 계속 증가중이다. 준비된 의사에게 유전체 검사는 이런 수요를 만족시킬 수 있도록 예방법과 치료 전략을 최적화할 수 있는 강력한 연장이 될 것이다.

